Effects of repeated transplantation of human umbilical cord mesenchymal stem cells in different time windows on silica-induced pulmonary fibrosis in rats
-
+ English摘要:目的
探讨人脐带间充质干细胞(human umbilical cord mesenchymal stem cells,HUCMSCs)在不同时间窗的重复移植对染矽尘大鼠肺纤维化的疗效。
方法将48只健康雄性SD大鼠随机分为4组:对照组、矽肺模型组、预防性干预组和治疗性干预组(每组12只)。采用非暴露式气管插管内灌注法,对照组注入0.5 mL生理盐水,其余各组均注入0.5 mL二氧化硅(SiO2)混悬液(50 mg/mL),1周后重复1次。首次染尘后,预防性干预组在第1、7、14、21天,治疗性干预组在第28、35、42、49天,经尾静脉缓慢注射0.5 mL HUCMSCs细胞悬液(3.0×109/L)。在第70天统一处理动物,以HE染色和Masson染色,观察肺组织病理改变并进行Aschcroft肺纤维化评分,检测肺系数、肺组织羟脯氨酸(hydroxyproline,Hyp)及转化生长因子-β1(TGF-β1)、血清白细胞介素-6(IL-6)的水平。
结果肺组织病理显示,对照组肺泡结构正常,其余各组肺脏有不同程度纤维化病变,矽肺模型组见细胞纤维性肉芽肿形成,预防性干预组和治疗性干预组与矽肺模型组比较,胶原纤维明显减少;Aschcroft评分、肺系数、肺组织Hyp和TGF-β1、血清IL-6比较,染尘各组均明显高于对照组(P < 0.01),而预防性干预组和治疗性干预组明显低于矽肺模型组(P < 0.01),预防性干预组和治疗性干预组之间以上指标差异均无统计学意义(P>0.05)。
结论采用重复注射HUCMSCs的方法,无论在以肺泡炎为主的阶段还是在以纤维化为主的阶段进行干预,均可以有效减轻矽尘导致的大鼠肺纤维化。
-
尘肺病(pneumoconiosis)是由于长期吸入致病性粉尘所引起的以肺组织弥漫性纤维化为主的疾病,是我国危害最严重和最常见的职业病,已成为我国严重的公共卫生问题,但迄今国内外均没有针对尘肺病纤维化的有效治疗药物和措施[1]。硅肺病(俗称矽肺病)是尘肺病中最常见、进展最快、危害最严重的一种类型。间充质干细胞(mesenchymal stem cell,MSCs)是一种源自中胚层的多能干细胞,具有多向分化潜能和免疫调节作用。多个动物实验发现,MSCs能够有效减轻肺纤维化动物模型的肺泡炎以及随后的肺纤维化,显示出MSCs有治疗尘肺病的潜质[2-4]。但目前的研究大多是在建模后短期内给予一次性的MSCs治疗,有一定的局限性。本研究经深圳市职业病防治院伦理委员会批准,采用气管内灌注游离SiO2建立大鼠矽肺模型,分别在大鼠肺损伤早期和晚期重复给予人脐带间充质干细胞(human umbilical cord mesenchymal stem cells,HUCMSCs)进行治疗,观察MSCs对肺纤维化的治疗作用,以期为MSCs治疗矽肺病提供一定的实验依据。
1. 材料与方法
1.1 材料
1.1.1 实验动物
无特定病原体(specific pathogen free,SPF)级健康雄性SD大鼠48只,体质量182.4 ~ 210.7 g,购自广东省医学实验动物中心,实验动物质量合格证号:NO.44007200046736,使用许可证号:SYXK(粤)2013-0002。大鼠饲养在广东省医学实验动物中心动物房,自由进食饮水,饲养条件符合《实验动物环境及设施》(GB 14925-2010)[5]的要求,实验通过广东省医学实验动物中心实验动物福利伦理审查。
1.1.2 主要试剂及仪器
游离SiO2粉尘,质量分数99%,80%的粒子直径为1 ~ 5 μm(美国Sigma公司)。第5代人脐带间充质干细胞(深圳市合一康生物科技股份有限公司)。羟脯氨酸(hydroxyproline,Hyp)测试盒(南京建成生物工程研究所); 大鼠转化生长因子-β1(transforming growth factor-β1,TGF-β1)、白细胞介素-6(interleukin-6,IL-6)酶联免疫(ELISA)试剂盒(武汉华美生物工程有限公司)。Infinite M1000 pro全波长酶标仪(瑞士Tecan公司); 超净工作台BCM-1000A(北京华威兴业科技有限公司); BS224S电子分析天平(德国Sartorius公司); Olympus BX43型生物显微镜及Olympus cellSens Dimension显微图像软件(日本Olympus公司); 小动物喉镜(上海玉研科学仪器有限公司)。
1.2 方法
1.2.1 SiO2混悬溶液配制方法
称取5 g游离SiO2粉尘,在超净工作台中加氯化钠(质量分数0.9%)注射液,配制成50 mg/mL的SiO2溶液,高压灭菌后加青霉素2 000 U/mL备用。
1.2.2 动物分组和处理
(1) 动物分组:采用随机数字表法将大鼠分为对照组、矽肺模型组、预防性干预组及治疗性干预组,每组12只,各组体质量无明显差异。
(2) 建立动物模型:取含戊巴比妥质量分数为3%的生理盐水溶液,从腹腔内注射(45 mg/kg),麻醉大鼠后将其固定,利用小动物喉镜暴露喉头,插入气管插管(18号静脉留置针改装)。模型组及干预组大鼠采用向气管内灌注0.5 mL SiO2混悬液,对照组采用向气管内灌注0.5 mL生理盐水溶液。一周后再次重复造模操作。
(3) HUCMSCs输注:首次染尘后,预防性干预组在第1、7、14、21天,治疗性干预组在第28、35、42、49天,经尾静脉缓慢注射HUCMSCs细胞悬液,细胞密度为3.0 × 109/L,0.5 mL/只。对照组及矽肺模型组同期经尾静脉注射磷酸缓冲盐溶液(phosphate buffer saline,PBS),0.5 mL/只。
(4) 标本采集:首次染尘后第70天统一处理动物。大鼠麻醉后,称量体质量,颈椎脱臼法处死,留取样本待测。
1.2.3 肺系数检测
摘取大鼠全肺,清除表面污物后,称量全肺湿质量,计算肺系数。肺系数(mg/g) =肺湿质量(mg)/体质量(g)。
1.2.4 肺组织病理学观察
右上肺组织经福尔马林(甲醛质量分数4%)固定24 h,经修块、流水冲洗、脱水、透明、浸蜡、石蜡包埋后,以5 μm厚度连续切片,切片经HE染色或Masson染色后封片,在光学显微镜下观察大鼠肺组织的形态学变化及纤维化程度等病理改变。按参考文献[2]的方法,进行Aschcroft肺纤维化分级:0级指正常肺组织; 1级指肺泡或支气管壁轻微增厚; 3级指肺泡或支气管壁中度增厚,但无肺组织结构的破坏; 5级指肺泡结构受到破坏,可见条索状纤维带或小范围纤维灶形成; 7级指肺组织结构严重破坏,形成大量纤维灶或产生“蜂窝状肺”; 8级指全视野纤维化病变; 2、4、6级介于相应的前后2个级别之间。Aschcroft评分按照其分级相应计为0 ~ 8分。每张切片随机取5个视野,由2位观察者进行双盲观察评分,取平均值作为最后得分。
1.2.5 肺组织Hyp、TGF-β1和血清IL-6水平测定
采用碱水解法测定肺组织Hyp水平。精确称取100 mg右下肺组织,严格按照试剂盒说明书制备组织水解液,逐步反应,用酶标仪在550 nm波长下测定光密度(optical density,OD)值,根据说明书提供的公式计算得出肺组织Hyp质量分数(μg/g)。采用ELISA双抗体夹心法检测肺组织TGF-β1和血清IL-6水平。精确称取大鼠的右下肺组织1.0 g制成含其质量分数为10%的组织匀浆液,离心半径12.5 cm、10 000 r/min离心10 min,吸取上清液,-20 ℃贮存备测TGF-β1; 腹主动脉采血5.0 mL,离心半径20 cm、3 000 r/min离心10 min后取血清,-20 ℃贮存备测IL-6。按照试剂盒说明书操作,用酶标仪分别测定在450 nm最大吸收波长和570 nm参考波长下的OD值,结果与标准曲线比较,计算样品的TGF-β1或IL-6水平。
1.2.6 统计学分析
采用SPSS 17.0软件进行统计学分析,计量资料经正态性检验,符合正态分布或近似正态分布者用均数±标准差(x ± s)表示,多组间比较采用单因素方差分析,组间两两比较采用LSD检验。P < 0.05为差异有统计学意义。
2. 结果
2.1 各组大鼠肺脏大体形态和肺系数
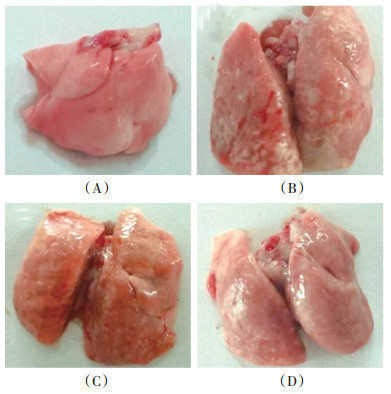
对照组肺脏表面光滑,呈粉红色,色泽均匀,质地弹性好; 矽肺模型组肺脏表面可见散在灰白色斑点,部分融合成不规则形斑块,颜色灰暗,质地较韧; 预防性干预组和治疗性干预组与矽肺模型组比较,肺脏表面灰白色斑点明显减少,颜色淡红,质地较软。见图 1。各组间肺系数差异均有统计学意义(P < 0.01);进一步两两比较,对照组肺系数低于其他组,预防性干预组和治疗性干预组低于矽肺模型组,以上差异均有统计学意义(P < 0. 01);预防性干预组和治疗性干预组之间肺系数差异无统计学意义(P > 0.05)。见表 1。
表 1 各组大鼠相关观察指标比较(x ± s) 组别 动物数量 肺系数/(mg/g) Aschcroft评分/分 肺组织Hyp水平/(mg/g) 肺组织TGF-β1水平/(ng/L) 血清IL-6水平/(ng/L) 对照组 12 4.45 ± 0.31 0.60 ± 0.16 0.70 ± 0.50 68.48 ± 5.83 33.96 ± 3.43 矽肺模型组 12 8.54 ± 0.47 a 5.82 ± 0.55 a 1.35 ± 0.13 a 123.10 ± 6.34 a 91.56 ± 3.74 a 预防性干预组 12 5.87 ± 0.82 a,b 3.93 ± 0.52 a,b 1.01 ± 0.41 a,b 98.9 ± 7.06 a,b 66.03 ± 5.89 a,b 治疗性干预组 12 5.64 ± 0.34 a,b 4.05 ± 0.62 a,b 0.93 ± 0.27 a,b 95.04 ± 4.67 a,b 60.45 ± 5.79 a,b F值 43.86 191.43 151.46 158.41 245.75 P值 < 0.01 < 0.01 < 0.01 < 0.01 < 0.01 [注] a与对照组比较,P < 0.01; b与模型组比较,P < 0.01 2.2 各组大鼠肺组织病理切片观察
HE染色结果显示,对照组肺泡结构正常,其余组肺脏有不同程度尘肺病变:矽肺模型组可见大量炎性细胞浸润,肺泡腔内有大量渗出液,肺泡间隔增厚,细胞纤维性肉芽肿形成; 与矽肺模型组比较,预防性干预组和治疗性干预组炎性细胞浸润、肺泡结构破坏、肺泡上皮增厚及细胞性结节均有所减少。Masson染色结果显示,对照组肺组织见正常少量蓝染胶原纤维支架; 矽肺模型组见大量胶原纤维沉着; 预防性干预组和治疗性干预组与矽肺模型组比较,胶原纤维明显减少。见图 2。各组间Aschcroft评分比较,差异有统计学意义(P < 0.01);进一步两两比较,对照组Aschcroft评分低于其他组别(P < 0.01),而预防性干预组和治疗性干预组低于矽肺模型组,以上差异均有统计学意义(P < 0.01);预防性干预组和治疗性干预组之间Aschcroft评分差异无统计学意义(P > 0.05)。见表 1。
2.3 各组大鼠肺组织Hyp、TGF-β1和血清IL-6水平比较
各组间肺组织Hyp、TGF-β1和血清IL-6水平比较,差异均有统计学意义(P < 0.01);进一步两两比较,对照组以上指标水平均低于其他组,预防性干预组和治疗性干预组均低于矽肺模型组,以上差异均有统计学意义(P < 0.01);预防性干预组与治疗性干预组之间以上指标差异无统计学意义(P > 0.05)。见表 1。
3. 讨论
硅肺病是长期吸入游离二氧化硅(SiO2)浓度较高的矿物性粉尘所导致的肺纤维化疾病。矽尘在肺内不易被清除,纤维化刺激持续存在,导致疾病不断进展,而博来霉素等诱导的肺纤维化具有自限性[6],因此,矽肺动物模型更适合于研究MSCs治疗肺纤维化,尤其是观察治疗尘肺病的效果[7-8]。包括本课题组前期研究在内的多个矽肺大鼠实验发现,采用气管内一次性灌注SiO2混悬液的方法,染尘后第1 ~ 2周肺组织以急性肺泡炎症反应为主,染尘第3 ~ 4周肺组织内出现明显的纤维组织增生[9-11]。本研究采用将SiO2混悬液分2次重复注射的方法建模,以减少染尘对实验动物的额外刺激。首次染尘第70天,矽肺模型组肺组织病理可见大量炎症细胞浸润,肺泡腔内大量渗出液,肺泡间隔增厚,细胞纤维性肉芽肿形成,肺系数和Aschcroft评分均高于对照组(P < 0.01),提示造模成功。
MSCs最早被发现存在于骨髓中,脐带间充质干细胞(umbilical cord mesenchymal stem cells,UCMSC)较骨髓间充质干细胞(bone marrow derived mesenchymal stem cell,BMMSC)表现出更类似于胚胎干细胞的基因表达谱,具有更快的自我扩增能力和更低的免疫原性[12-14]。脐带本来就是一个被遗弃的组织,来源充足,HUCMSCs采集过程不会给患者带来痛苦,因此有更广阔的应用前景。本研究采用HUCMSCs进行移植。
动物实验研究发现,采用单次尾静脉注射MSCs治疗染矽尘大鼠,在以肺泡炎为主的阶段进行干预效果明显,而在以肺纤维为主的阶段才干预,效果明显减弱[15],甚至不明显[16]。本课题组前期研究也得出类似结论,并发现MSCs的抗纤维化作用会随时间推移而减弱[7-8]。但临床上就诊并接受治疗的矽肺患者均已处于以肺纤维化为主的阶段,因此目前的研究不能满足临床实际需要。本研究采用重复尾静脉注射MSCs的方法分别在以肺泡炎为主的阶段(预防性干预组)和以肺纤维为主的阶段(治疗性干预组)进行干预,观察MSCs抗肺纤维化的效果。结果发现,预防性干预组和治疗性干预组的肺组织病理切片HE和Masson染色观察稍好于矽肺模型组,肺脏大体形态、肺系数、Aschcroft评分均好于矽肺模型组(P < 0.01);而预防性干预组与治疗性干预组比较,差异无统计学意义(P > 0.05)。结果提示,不论在以肺泡炎为主的阶段还是在以肺纤维为主的阶段,采用重复尾静脉注射MSCs抗矽肺肺纤维化均有效。Hyp是机体胶原蛋白中一种主要的氨基酸,在其他蛋白中浓度极低或不存在,组织中Hyp的水平能体现胶原沉积水平,反映纤维化的程度[17]。本研究中四组大鼠的肺组织Hyp水平与肺组织病理改变相符,进一步证实了MSCs抗肺纤维化效果。由于本研究只观察了首次染尘后第70天的情况,因此远期效果还需要进一步验证。
尘肺病发病机制复杂,不仅存在肺脏局部病理改变,也存在免疫功能的紊乱[18]。MSCs治疗肺纤维化的可能机制有:(1) MSCs迁移并定植到受损的肺组织[19-21],分化成为包括Ⅰ型和Ⅱ型肺泡上皮细胞、内皮细胞等,促进组织修复[22-23]; (2) MSCs在受损肺组织定植率低[22, 25],更多的是发挥免疫调节作用[22],减轻组织炎症反应,从而减少组织纤维化等。TGF-β1是一种较强的促纤维化细胞因子,既可以上调致纤维化基因的表达和胶原的分泌,以促进细胞外基质的沉积,又可以下调蛋白酶的分泌、增加降解蛋白酶抑制剂的合成,进而抑制细胞外基质的降解,还可以促进成纤维细胞的增殖,在肺纤维化的发病机制中起着关键的作用[26-27]。IL-6是一种促炎因子,可刺激成纤维细胞中的IL-6转运信号,促进成纤维细胞增殖的作用,增加细胞外基质蛋白的产生,参与纤维化的形成[28]。本研究发现,矽肺模型组、预防性干预组和治疗性干预组肺组织TGF-β1和血清IL-6水平均高于对照组(P < 0.01),预防性干预组和治疗性干预组则低于矽肺模型组(P < 0.01),提示通过下调TGF-β1[3, 29]、IL-6的水平[4, 30],可能是MSCs抗肺纤维化的机制之一。
SiO2颗粒进入肺组织后,首先被肺泡巨噬细胞(alveolar macrophage,AM)吞噬,AM活化并产生大量的细胞因子和致纤维化因子,包括TGF-β1、IL-6等。AM吞噬矽尘粒子后崩解死亡,所释放的矽尘颗粒再被其他AM吞噬,形成AM吞噬和死亡的恶性循环过程和由此导致的肺组织持续存在的慢性炎症[31]。重复注射HUCMSCs可能正是针对矽肺发病中肺组织内持续存在的慢性炎症而发挥作用。
综上所述,在硅肺病发展过程中,采用重复注射HUCMSCs的方法,不论在以肺泡炎为主的阶段还是在以纤维化为主的阶段进行干预,均有抗纤维化效果; 通过下调TGF-β1、IL-6的水平,可能是MSCs抗肺纤维化的机制之一。
-
表 1 各组大鼠相关观察指标比较
(x ± s) 组别 动物数量 肺系数/(mg/g) Aschcroft评分/分 肺组织Hyp水平/(mg/g) 肺组织TGF-β1水平/(ng/L) 血清IL-6水平/(ng/L) 对照组 12 4.45 ± 0.31 0.60 ± 0.16 0.70 ± 0.50 68.48 ± 5.83 33.96 ± 3.43 矽肺模型组 12 8.54 ± 0.47 a 5.82 ± 0.55 a 1.35 ± 0.13 a 123.10 ± 6.34 a 91.56 ± 3.74 a 预防性干预组 12 5.87 ± 0.82 a,b 3.93 ± 0.52 a,b 1.01 ± 0.41 a,b 98.9 ± 7.06 a,b 66.03 ± 5.89 a,b 治疗性干预组 12 5.64 ± 0.34 a,b 4.05 ± 0.62 a,b 0.93 ± 0.27 a,b 95.04 ± 4.67 a,b 60.45 ± 5.79 a,b F值 43.86 191.43 151.46 158.41 245.75 P值 < 0.01 < 0.01 < 0.01 < 0.01 < 0.01 [注] a与对照组比较,P < 0.01; b与模型组比较,P < 0.01 -
[1] 中华预防医学会劳动卫生与职业病分会职业性肺部疾病学组.尘肺病治疗中国专家共识(2018年版)[J].环境与职业医学, 2018, 35(8):677-689. http://d.old.wanfangdata.com.cn/Periodical/ldyx201808001 [2] 赵娜, 吴洁, 宋向荣, 等.骨髓间充质干细胞治疗矽肺小鼠肺纤维化效果[J].中国职业医学, 2017, 44(6):657-663. http://d.old.wanfangdata.com.cn/Periodical/zgzyyx201706001 [3] 左万里, 邓冏睿, 黄积雄, 等.间充质干细胞对肺纤维化的治疗作用[J].中华实验外科杂志, 2018, 35(3):492-496. doi: 10.3760/cma.j.issn.1001-9030.2018.03.030 [4] 吴洁, 王海兰, 宋向荣.骨髓间充质干细胞减轻染矽尘小鼠肺泡炎机制研究[J].中国职业医学, 2016, 43(4):393-399. http://d.old.wanfangdata.com.cn/Periodical/zgzyyx201604001 [5] 全国实验动物标准化技术委员会.实验动物环境及设施: GB 14925-2010[S].北京: 中国标准出版社, 2011. [6] MOORE B B, HOGABOAM C M. Murine models of pulmonary fibrosis[J]. Am J Physiol Lung Cell Mol Physiol, 2008, 294(2):L152-L160. doi: 10.1152/ajplung.00313.2007
[7] 陈志军, 黄惠霞, 谢英, 等.骨髓间充质干细胞移植对矽肺大鼠肺纤维化的作用[J].重庆医学, 2017, 46(12):1585-1587. doi: 10.3969/j.issn.1671-8348.2017.12.001 [8] 陈志军, 张健杰, 黄惠霞, 等.不同时期骨髓间充质干细胞移植对矽肺大鼠CD4+ CD25+调节性T细胞的影响[J].职业与健康, 2016, 32(22):3067-3070, 3074. http://d.old.wanfangdata.com.cn/Periodical/zyyjk201622013 [9] LAKATOS H F, BURGESS H A, THATCHER T H, et al. Oropharyngeal aspiration of a silica suspension produces a superior model of silicosis in the mouse when compared to intratracheal instillation[J]. Exp Lung Res, 2006, 32(5):181-199. http://www.wanfangdata.com.cn/details/detail.do?_type=perio&id=10.1080/01902140600817465
[10] 李春红, 朱文, 董西方, 等.实验性矽肺模型大鼠外周血CD4+CD25+ Foxp3+调节性T细胞的变化及意义[J].环境与职业医学, 2010, 27(8):480-482. http://d.old.wanfangdata.com.cn/Periodical/ldyx201008008 [11] 朱文, 沙泉, 董西方, 等.实验性矽肺大鼠肺组织中Th1/Th2型细胞因子的变化及意义[J].安徽医药, 2010, 14(9):1034-1036. doi: 10.3969/j.issn.1009-6469.2010.09.019 [12] HSIEH J Y, FU Y S, CHANG S J, et al. Functional module analysis reveals differential osteogenic and stemness potentials in human mesenchymal stem cells from bone marrow and Wharton's jelly of umbilical cord[J]. Stem Cells Dev, 2010, 19(12):1895-1910. doi: 10.1089/scd.2009.0485
[13] 弓勋, 云升.间充质干细胞的生物学特性及应用[J].中国医学工程, 2018, 26(12):40-44. http://d.old.wanfangdata.com.cn/Periodical/gdyx201701043 [14] DING D C, CHANG Y H, SHYU W C, et al. Human umbilical cord mesenchymal stem cells:a new era for stem cell therapy[J]. Cell Transplant, 2015, 24(3):339-347. doi: 10.3727/096368915X686841
[15] 张应洵, 黄明, 陆丰荣, 等.骨髓间充质干细胞对染矽尘大鼠肺纤维化干预作用[J].中国职业医学, 2017, 45(2):121-126. http://d.old.wanfangdata.com.cn/Periodical/zgzyyx201702001 [16] 朱会兴, 高俊玲, 赵曼曼, 等.不同时间骨髓间充质干细胞移植对大鼠矽肺纤维化形成的影响[J].中国免疫学杂志, 2015, 31(2):193-196. doi: 10.3969/j.issn.1000-484X.2015.02.012 [17] YANG D, YUAN W, LV C, et al. Dihydroartemisinin suppresses inflammation and fibrosis in bleomycine induced pulmonary fibrosis in rats[J]. Int J Clin Exp Pathol, 2015, 8(2):1270-1281.
[18] MAEDA M, NISHIMURA Y, KUMAGAI N, et al. Dysregulation of the immune system caused by silica and asbestos[J]. J Immunotoxicol, 2010, 7(4):268-278. doi: 10.3109/1547691X.2010.512579
[19] ZHANG F, LEONG W, SU K, et al. A transduced living hyaline cartilage graft releasing transgenic stromal cell-derived factor-1 inducing endogenous stem cell homing in vivo[J]. Tissue Eng Part A, 2013, 19(9/10):1091-1099. http://www.wanfangdata.com.cn/details/detail.do?_type=perio&id=ecbd01aa85b67a3a5aeb36be2382ba07
[20] DU Z, WEI C, YAN J, et al. Mesenchymal stem cells over expressing CX-C chemokine receptor type 4 improve early liver regeneration of small-for-size liver grafts[J]. Liver Transpl, 2013, 19(2):215-225. doi: 10.1002/lt.23577
[21] MARQUEZ-CURTIS L A, JANOWSKA-WIECZOREK A. Enhancing the migration ability of mesenchymal stromal cells by targeting the SDF-1/CXCR4 axis[J]. Biomed Res Int, 2013, 2013:561098. http://www.wanfangdata.com.cn/details/detail.do?_type=perio&id=Doaj000002872568
[22] ABREU S C, ANTUNES M A, PELOSI P, et al. Mechanisms of cellular therapy in respiratory diseases[J]. Intensive Care Med, 2011, 37(9):1421-1431. http://d.old.wanfangdata.com.cn/OAPaper/oai_pubmedcentral.nih.gov_3360792
[23] 黄坤, 吴晓梅, 王欣燕, 等.骨髓间充质干细胞向肺泡细胞转化的实验研究[J].中国呼吸与危重监护杂志, 2011, 10(6):572-576. doi: 10.3969/j.issn.1671-6205.2011.06.013 [24] ARAUJO I M, ABREU S C, MARON-GUTIERREZ T, et al. Bone marrow-derived mononuclear cell therapy in experimental pulmonary and extrapulmonary acute lung injury[J]. Crit Care Med, 2010, 38(8):1733-1741. doi: 10.1097/CCM.0b013e3181e796d2
[25] AKRAM K M, SAMAD S, SPITERI M A, et al. Mesenchymal stem cells promote alveolar epithelial cell wound repair in vitro through distinct migratory and paracrine mechanisms[J]. Respir Res, 2013, 14(2):258-264. http://d.old.wanfangdata.com.cn/OAPaper/oai_pubmedcentral.nih.gov_3598763
[26] LI X X, LI N, BAN C J, et al. Idiopathic pulmonary fibrosis in relation to gene polymorphisms of transforming growth factor-β1 and plasminogen activator inhibitor 1[J]. Chin Med J(Engl), 2011, 124(13):1923-1927. http://www.wanfangdata.com.cn/details/detail.do?_type=perio&id=zhcmj201113001
[27] 王红阳, 刘晨, 王雁, 等.人脐血间充质干细胞治疗大鼠肺纤维化的实验研究[J].中华劳动卫生职业病杂志, 2013, 31(9):675-680. doi: 10.3760/cma.j.issn.1001-9391.2013.09.008 [28] LE T T, KARMOUTY-QUINTANA H, MELICOFF E, et al. Blockade of IL-6 trans signaling attenuates pulmonary fibrosis[J]. J Immunol, 2014, 193(7):3755-3768. http://www.wanfangdata.com.cn/details/detail.do?_type=perio&id=94837992c9be6833f1e4767caff20b4a
[29] 陶金, 李庆伦, 马晓薇, 等.人胎盘胎儿来源间充质干细胞通过下调髓样分化因子88和转化生长因子β信号通路减轻小鼠肺纤维化[J].细胞与分子免疫学杂志, 2016, 32(10):1347-1351. http://d.old.wanfangdata.com.cn/Periodical/xbyfzmyxzz201610011 [30] 阳成成, 吴晓梅.骨髓间充质干细胞对大鼠肺纤维化的抑制作用[J].中西医结合心脑血管病杂志, 2016, 14(10):1091-1094. doi: 10.3969/j.issn.1672-1349.2016.10.011 [31] 孔海霞, 陈娟娟, 刘伟, 等.肺巨噬细胞在矽肺肺纤维化发生发展中的作用[J].中华劳动卫生职业病杂志, 2012, 30(4):318-320. doi: 10.3760/cma.j.issn.1001-9391.2012.04.024





 下载:
下载:

