Effect of bone marrow mesenchymal stem cells on recovery of skin burn in C57BL/6J mice
-
+ English摘要:目的
探讨骨髓间充质干细胞(bone marrow mesenchymal stem cells,BMSCs)对小鼠皮肤烫伤的促修复作用,为临床采用BMSCs治疗烫伤提供依据。
方法以3周龄C57BL/6J小鼠的骨髓细胞悬液体外扩增培养BMSCs。将36只10周龄C57BL/6J小鼠随机分为局部细胞移植组、尾静脉细胞移植组和平行对照组(每组12只),建立皮肤烫伤模型。小鼠皮肤烫伤损伤模型建立成功1 h后,将BMSCs通过皮下和尾静脉分别注射到两个细胞移植组中,平行对照组注射生理盐水。观察动物创面变化,计算21 d后的创面愈合率、检测炎症因子变化和皮肤形态学变化。
结果分离培养的BMSCs增殖旺盛,能够多向分化为成骨细胞、成软骨细胞和成脂细胞。局部细胞移植组和尾静脉细胞移植组的创面愈合率在21 d后达到98.2%和99.0%,其差异无统计学意义(P > 0.05);而平行对照组愈合率在7 d后明显低于两个细胞移植组(P < 0.05)。BMSCs移植后,在第3天和第7天后,两个细胞移植组白细胞和白细胞介素-6(IL-6)水平明显低于平行对照组(P < 0.05);在3 d、7 d和14 d后,两个细胞移植组C反应蛋白和肿瘤坏死因子-α(TNF-α)水平明显低于平行对照组(P < 0.05);但21 d后各炎症因子水平在各组间差异无统计学意义(P > 0.05)。两个细胞移植组的皮肤形态学在21 d后胶原纤维丰富,皮肤组织结构清晰,而平行对照组可见炎性细胞浸润、胶原排列紊乱和充血现象。
结论皮肤烫伤模型移植BMSCs后,后者可提高宿主C57BL/6J小鼠的皮肤烫伤恢复能力。
-
烫伤作为一种并不罕见的疾病,一直困扰着不少临床工作者。皮肤缺损创面的覆盖与修复,是临床医师倍感棘手的问题。大面积皮肤缺损患者,由于自体皮源不足,很难满足尽快封闭创面的需求。在治疗皮肤创伤的应用中,干细胞的表现越来越引起人们关注。干细胞分为胚胎干细胞和成体干细胞两大类[1],它们都可以用于损伤皮肤组织的修复和再生。胚胎干细胞虽有较强的自我更新能力,但其来源不足且伦理问题突出,因此,成体干细胞逐渐成为研究重点。其中骨髓间充质干细胞(bone marrow mesenchymal stem cells,BMSCs)在体内和体外均具备分化潜能,是治疗皮肤损伤的重要细胞,且易于获取和培养,具有多向分化潜能、免疫原性低等特点,是目前皮肤创伤修复中主要的异体细胞种类[2]。国内有研究显示BMSCs通过旁分泌等途径发挥其免疫调节和抗纤维化作用,对纤维化疾病有明显抑制作用,并在皮肤瘢痕防治中取得肯定、良好的效果[3-4]。Zheng等[5]研究发现,BMSCs可以分泌转化生长因子β1、基质细胞衍生因子-1(stromal cell derived factor-1,SDF-1)和前列腺素E2,抑制炎症反应,增加细胞趋化性与增殖能力,抑制纤维化和瘢痕形成,这为细胞治疗皮肤烫伤损伤奠定了基础。本研究拟将BMSCs通过局部和尾静脉移植到皮肤烫伤的小鼠模型体内,观察BMSCs对皮肤烫伤是否有促修复作用,为临床采用BMSCs创伤治疗提供依据。
1. 材料与方法
1.1 材料
1.1.1 动物与分组
由山东第一医科大学实验动物部提供本研究所用小鼠,其中健康3周龄C57BL/6J小鼠3只,用于提取BMSCs;健康10周龄C57BL/6J小鼠36只,体重20 ~ 22 g。按照完全随机设计原则,随机分为3组(各12只):局部细胞移植组、尾静脉细胞移植组和平行对照组。
1.1.2 实验试剂
低糖DMEM(Dulbecco's modified eagle medium)培养基(GIBACO)、胎牛血清(赛业生物)、胰蛋白酶(赛默飞)、Percoll工作液(Pharmacia)、白细胞计数试剂盒(Sigma)、C-反应蛋白检测试剂盒(九邦生物)、ELISA试剂盒(索莱宝)、HE染色试剂盒(索莱宝)等。
1.2 方法
1.2.1 BMSCs的培养和鉴定
选用3周龄C57BL/6J幼鼠3只,脱臼处死后放入体积分数为75%的酒精中浸泡5 min。无菌条件下,快速取出双侧股骨,用含DMEM培养液冲洗骨髓腔,收集骨髓细胞悬液。Percoll工作液分离,200目滤网过滤成单细胞,接种于培养瓶中,其培养体系为含20%(体积分数)的胎牛血清DMEM培养液,放置在37 ℃饱和CO2湿度孵箱静置培养。
细胞分化实验:取第3代BMSCs,接种到有盖玻片6孔培养板中。当细胞融合到80% ~ 90%时,加成骨细胞分化培养液、成软骨细胞分化培养液和脂肪细胞分化培养液。诱导28 d后分别对成骨细胞、成软骨细胞、成脂细胞做碱性磷酸酶染色、甲苯胺蓝染色和油红染色。
1.2.2 建立小鼠皮肤烫伤损伤模型
用质量分数为3%的戊巴比妥以1.0 mL/kg的剂量麻醉小鼠后,3组小鼠背部皮肤备皮,碘伏消毒。将铁模烧成红色,待测底(直径1.5 cm)中心温度达100 ~ 110 ℃时(使用MT4便携式可见红外温度计测定温度)置于小鼠背部25 s,统一制作成直径为1.5 cm的深Ⅱ度烫伤模型。
1.2.3 BMSCs移植
小鼠皮肤烫伤损伤模型建立成功1 h后,局部细胞移植组、尾静脉细胞移植组分别通过烫伤处皮下和尾静脉注射0.5 mL的2 × 106 /mL BMSCs悬液,平行对照组尾静脉注射0.5 mL的生理盐水。皮下注射采用5点注射法,每个点皮下注射0.1 mL细胞悬液。
1.2.4 标本采集及检测
(1) 观察小鼠皮肤创面变化、肉芽组织生长和创面愈合情况;创面愈合率=(初始创面面积-测量当日面积)/初始创面面积× 100%。
(2) 小鼠不同时相点通过尾静脉采血约0.5 mL行炎症因子检测,白细胞和C反应蛋白采用免疫浊度自动分析法检测,IL-6和TNF-α采用ELISA法测量。
(3) 21 d后取小鼠烫伤处皮肤固定包埋,做皮肤组织切片并进行HE染色。
1.2.5 统计学分析
采用SPSS 24.0统计软件进行分析,所有实验室计量指标采用均数±标准差(x ± s)表示。由于愈合率为非正态分布资料,经平方根反正弦转化后接近正态,再进行统计分析。本研究采用重复测量设计资料的方差分析进行数据处理(组间和不同时间点的多重比较采用LSD法),以P < 0.05为差异有统计学意义。
2. 结果
2.1 BMSCs的扩增培养与鉴定
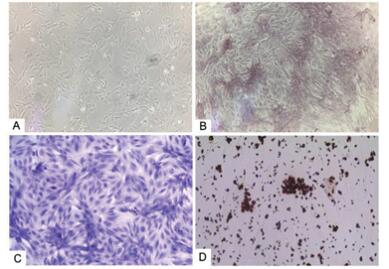
BMSCs接种24 h后便可见少数细胞贴壁,3 ~ 4 d后见细胞集落形成。传代后细胞形态分布均一,且生长速度大大提高,取培养3代后细胞置于镜下观察,细胞形态稳定清晰,呈梭形分布(图 1A)。经成骨、成软骨和成脂分化培养液分别诱导染色后,BMSCs胞浆中分别出现了浅棕色至棕黑色(图 1B)、蓝色(图 1C)和红色颗粒(图 1D),提示BMSCs实现了向成骨细胞、成软骨细胞和成脂细胞的定向分化。
2.2 BMSCs移植后创面的愈合率
3 d后,3组C57BL/6J小鼠精神萎靡,少动,状态差;7 d后,平行对照组小鼠精神状态一般,而两组细胞移植组小鼠在外观体征和行为活动上已与正常小鼠无异;14 d后,3组小鼠精神状态和行为特征均与正常小鼠无异。3组小鼠均成活到实验结束,皮肤创面逐日缩小,无感染现象,3组小鼠皮肤创面的愈合率见表 1。3 d后3组小鼠皮肤创面愈合率差异无统计学意义(P > 0.05);7 d后不同时间点移植组的愈合率均高于对照组,差异有统计学意义(P < 0.05),但局部细胞移植组与尾静脉细胞移植组在愈合率方面差异无统计学意义(P > 0.05)。另外,3组的愈合率随时间逐渐升高,各时间点的愈合率差异有统计学意义(P < 0.05);且细胞移植与时间存在交互效应(F = 31.629,P < 0.01),即随时间变化BMSCs对愈合率有影响。
表 1 3组小鼠皮肤创面愈合率(%) 组别 n 3 d后 7 d后 14 d后 21 d后 局部细胞
移植组12 16.9 ± 3.5 49.3 ± 8.1a,b 80.8 ± 11.9a,b,c 98.2 ± 2.7a,b,c,d 尾静脉细
胞移植组12 15.9 ± 3.9 51.3 ± 8.8a,b 82.6 ± 10.8a,b,c 99.0 ± 2.1a,b,c,d 平行
对照组12 11.3 ± 3.3 23.2 ± 5.5 b 50.8 ± 7.9 b,c 75.8 ± 5.5b,c,d 注:F组间= 359.341,P < 0.01;F时间= 2 084.575,P < 0.01;a与平行对照组相比,P < 0.05;b与3 d时相比,P < 0.05;c与7 d时相比,P < 0.05;d与14 d时相比,P < 0.05。 2.3 BMSCs移植后炎症因子变化趋势
BMSCs移植小鼠后,白细胞和白细胞介素-6(IL-6)在3 d和7 d后,两个细胞移植组与平行对照组相比,差异有统计学意义(P < 0.05),其水平均低于平行对照组(见表 2和表 3);而C反应蛋白和TNF-α在3 d、7 d和14 d,两个细胞移植组与平行对照组相比,差异有统计学意义(P < 0.05),其水平均低于平行对照组(见表 4和表 5);但随着时间延长,21 d后各炎症因子水平在各组间差异无统计学意义(P > 0.05)。另外,3组的白细胞计数和C反应蛋白随时间逐渐升高,各时间点的白细胞计数和C反应蛋白差异有统计学意义(P < 0.05);其细胞移植与时间存在交互效应(F = 12.017和18.193,P < 0.01),即随时间变化BMSCs对白细胞计数和C反应蛋白有影响。见表 2、表 3。3组的IL-6和TNF-α虽在某些时间点之间差异无统计学意义(P > 0.05),但总体表现为先上升后下降的趋势;其细胞移植与时间也存在交互效应(F = 4.935、2.709,P < 0.05),即随时间变化BMSCs对IL-6和TNF-α有影响。见表 3、表 5。
表 2 3组小鼠不同时间点白细胞计数水平(× 109/L) 组别 n 3 d后 7 d后 14 d后 21 d后 局部细胞
移植组6 9.83 ± 0.46a 9.12 ± 0.53a,b 9.52 ± 0.37 8.36 ± 0.62b,c,d 尾静脉细
胞移植组6 8.62 ± 1.06a,b 51.3 ± 8.8a,b 9.63 ± 0.93 8.99 ± 0.88b 平行
对照组6 13.92 ± 1.01 11.17 ± 1.08b 9.30 ± 0.61b,c 8.64 ± 0.98b,c 注:F组间= 19.770,P < 0.01;F时间= 34.120,P < 0.01;a与平行对照组相比,P < 0.05;b与3 d时相比,P < 0.05;c与7 d时相比,P < 0.05;d与14 d时相比,P < 0.05。 表 3 三组小鼠不同时间点IL-6水平(pg/mL) 组别 n 3 d后 7 d后 14 d后 21 d后 局部细胞
移植组6 25.26 ± 1.38a 25.28 ± 1.88a 28.30 ± 1.74b,c 25.25 ± 1.21d 尾静脉细
胞移植组6 26.73 ± 2.02a 26.84 ± 1.71a 28.85 ± 1.91b 26.09 ± 1.31d 平行
对照组6 31.27 ± 1.45 32.08 ± 2.36 30.27 ± 1.44 26.73 ± 1.33b,c,d 注:F组间= 30.706,P < 0.01;F时间= 11.558,P < 0.01;a与平行对照组相比,P < 0.05;b与3 d时相比,P < 0.05;c与7 d时相比,P < 0.05;d与14 d时相比,P < 0.05。 表 4 3组小鼠不同时间点C反应蛋白水平(mg/L) 组别 n 3 d后 7 d后 14 d后 21 d后 局部细胞
移植组6 2.18 ± 0.29a 1.88 ± 0.37a 1.83 ± 0.19b 1.57 ± 0.13b 尾静脉细
胞移植组6 2.15 ± 0.34a 1.84 ± 0.43a 1.47 ± 0.21a,b 1.59 ± 0.10b 平行
对照组6 4.18 ± 0.48 2.72 ± 0.22b 1.94 ± 0.22b,c 1.61 ± 0.13b,c 注:F组间= 83.746,P < 0.01;F时间= 61.773,P < 0.01;a与平行对照组相比,P < 0.05;b与3 d时相比,P < 0.05;c与7 d时相比,P < 0.05;d与14 d时相比,P < 0.05。 表 5 三组小鼠不同时间点TNF-α水平(pg/mL) 组别 n 3 d后 7 d后 14 d后 21 d后 局部细胞
移植组6 11.48 ± 1.42a 13.45 ± 0.77a,b 12.60 ± 1.11a 9.27 ± 1.05b,c,d 尾静脉细
胞移植组6 11.91 ± 0.60a 14.39 ± 0.96a,b 12.83 ± 1.40a,c 9.35 ± 0.50b,c,d 平行
对照组6 15.15 ± 0.76 17.52 ± 0.86b 15.61 ± 1.37c 10.17 ± 1.00b,c,d 注:F组间= 140.736,P < 0.01;F时间= 78.134,P < 0.01;a与平行对照组相比,P < 0.05;b与3 d时相比,P < 0.05;c与7 d时相比,P < 0.05;d与14 d时相比,P < 0.05。 2.4 BMSCs移植21 d后皮肤组织学变化
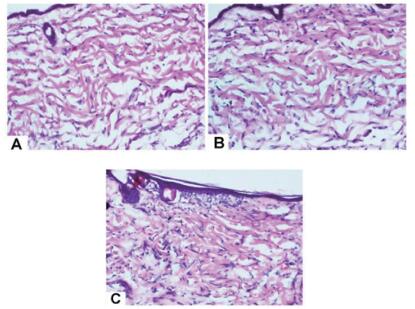
取3组小鼠21 d后烫伤部位的皮肤组织行病理切片,经HE染色发现,局部细胞移植组和尾静脉细胞组皮肤组织结构清晰,其胶原纤维丰富,排列规律,可见少量的炎症细胞存在,而平行对照组可见大量炎性细胞浸润、组织有凝固型坏死、胶原排列紊乱和充血现象。见图 2。
3. 讨论
BMSCs具有增殖性强、多向分化的可塑性特点,已在很多疾病取得了可喜的效果[6]。本研究分离培养的BMSCs体积小,呈梭形,增殖迅速。经多向细胞分化实验,成功将其诱导为成骨细胞、成软骨细胞和成脂细胞,证实了本研究培养的细胞是BMSCs。实验创面愈合率显示,0 ~ 3 d时3组的创面愈合率差异无统计学意义(P > 0.05),7 d后局部细胞移植组和尾静脉细胞移植组的创面愈合率显著高于平行对照组(P < 0.05),两个细胞移植组的创面愈合率在21 d后接近100%,而平行对照组创面愈合率为75.8%。Zhang等[7]和Guo等[8]在BMSCs修复大鼠皮肤烧伤模型中显示BMSCs能显著提高大鼠创面皮肤愈合率。本研究中BMSCs移植组在愈合速度上优于对照组,进一步揭示BMSCs能显著促进烫伤创面的愈合,其研究结果与其类似。
有研究表明皮肤肥大细胞早期参与创伤的炎症反应和后期的组织成纤维化过程,通过释放一些炎症介质来实现对皮肤创伤的修复[9],所以在观察小鼠创面愈合率变化的同时,我们取小鼠血清样本检测炎症因子含量变化,进一步探究BMSCs促创面恢复的作用机制。通过实验比较发现局部细胞移植组和尾静脉细胞移植组的白细胞计数在最初3 ~ 7 d时均低于平行对照组水平,而在14 ~ 21 d时3组白细胞计数水平差异无统计学意义(P > 0.05),且波动范围较小,可初步认为移植BMSCs后炎症反应得到了有效控制。局部细胞移植组和尾静脉细胞移植组的其他炎症因子在最初的14 d内水平均低于平行对照组,而在21 d后3组炎症因子水平差异无统计学意义(P > 0.05),这说明在皮肤创面恢复条件一定的情况下,经BMSCs移植可有效抑制早期的炎症反应,防止创面进一步损伤。
通过组织形态学观察结果也显示BMSCs移植C57BL/6J小鼠后减轻了皮肤组织损伤,21 d后组织学基本恢复正常,而平行对照组仍可见炎性细胞浸润、胶原排列紊乱等现象。其可能原因是BMSCs具有向成纤维细胞、毛细血管内皮细胞、表皮细胞等细胞分化的潜能[10],并通过旁分泌形式分泌抗损伤修复细胞因子[11],加速了新生组织修复所需要的营养和血供,达到了组织修复的作用[12]。
本研究进一步证实BMSCs在体外具有旺盛的增殖能力和多向分化能力;移植皮肤烫伤模型小鼠后,可显著改善皮肤创面愈合率,并通过降低烫伤后炎症因子抑制继发的炎症反应,促进创面修复。
由于需要在不同时间点采样,此次研究所使用的小鼠数量过多,在今后研究中将充分考虑动物福利。另外,实验也表明BMSCs促进皮肤愈合的作用机制可能和炎症反应有关,能在短时间内有效抑制炎症因子的产生从而促进伤口愈合,但是否有其他因素影响BMSCs的促愈合效果,还需更多的研究。综上所述,移植BMSCs能促进烫伤皮肤创面的早期愈合,其愈合效果较对照组具有明显差异。
作者声明 本文无实际或潜在的利益冲突 -
表 1 3组小鼠皮肤创面愈合率
(%) 组别 n 3 d后 7 d后 14 d后 21 d后 局部细胞
移植组12 16.9 ± 3.5 49.3 ± 8.1a,b 80.8 ± 11.9a,b,c 98.2 ± 2.7a,b,c,d 尾静脉细
胞移植组12 15.9 ± 3.9 51.3 ± 8.8a,b 82.6 ± 10.8a,b,c 99.0 ± 2.1a,b,c,d 平行
对照组12 11.3 ± 3.3 23.2 ± 5.5 b 50.8 ± 7.9 b,c 75.8 ± 5.5b,c,d 注:F组间= 359.341,P < 0.01;F时间= 2 084.575,P < 0.01;a与平行对照组相比,P < 0.05;b与3 d时相比,P < 0.05;c与7 d时相比,P < 0.05;d与14 d时相比,P < 0.05。 表 2 3组小鼠不同时间点白细胞计数水平
(× 109/L) 组别 n 3 d后 7 d后 14 d后 21 d后 局部细胞
移植组6 9.83 ± 0.46a 9.12 ± 0.53a,b 9.52 ± 0.37 8.36 ± 0.62b,c,d 尾静脉细
胞移植组6 8.62 ± 1.06a,b 51.3 ± 8.8a,b 9.63 ± 0.93 8.99 ± 0.88b 平行
对照组6 13.92 ± 1.01 11.17 ± 1.08b 9.30 ± 0.61b,c 8.64 ± 0.98b,c 注:F组间= 19.770,P < 0.01;F时间= 34.120,P < 0.01;a与平行对照组相比,P < 0.05;b与3 d时相比,P < 0.05;c与7 d时相比,P < 0.05;d与14 d时相比,P < 0.05。 表 3 三组小鼠不同时间点IL-6水平
(pg/mL) 组别 n 3 d后 7 d后 14 d后 21 d后 局部细胞
移植组6 25.26 ± 1.38a 25.28 ± 1.88a 28.30 ± 1.74b,c 25.25 ± 1.21d 尾静脉细
胞移植组6 26.73 ± 2.02a 26.84 ± 1.71a 28.85 ± 1.91b 26.09 ± 1.31d 平行
对照组6 31.27 ± 1.45 32.08 ± 2.36 30.27 ± 1.44 26.73 ± 1.33b,c,d 注:F组间= 30.706,P < 0.01;F时间= 11.558,P < 0.01;a与平行对照组相比,P < 0.05;b与3 d时相比,P < 0.05;c与7 d时相比,P < 0.05;d与14 d时相比,P < 0.05。 表 4 3组小鼠不同时间点C反应蛋白水平
(mg/L) 组别 n 3 d后 7 d后 14 d后 21 d后 局部细胞
移植组6 2.18 ± 0.29a 1.88 ± 0.37a 1.83 ± 0.19b 1.57 ± 0.13b 尾静脉细
胞移植组6 2.15 ± 0.34a 1.84 ± 0.43a 1.47 ± 0.21a,b 1.59 ± 0.10b 平行
对照组6 4.18 ± 0.48 2.72 ± 0.22b 1.94 ± 0.22b,c 1.61 ± 0.13b,c 注:F组间= 83.746,P < 0.01;F时间= 61.773,P < 0.01;a与平行对照组相比,P < 0.05;b与3 d时相比,P < 0.05;c与7 d时相比,P < 0.05;d与14 d时相比,P < 0.05。 表 5 三组小鼠不同时间点TNF-α水平
(pg/mL) 组别 n 3 d后 7 d后 14 d后 21 d后 局部细胞
移植组6 11.48 ± 1.42a 13.45 ± 0.77a,b 12.60 ± 1.11a 9.27 ± 1.05b,c,d 尾静脉细
胞移植组6 11.91 ± 0.60a 14.39 ± 0.96a,b 12.83 ± 1.40a,c 9.35 ± 0.50b,c,d 平行
对照组6 15.15 ± 0.76 17.52 ± 0.86b 15.61 ± 1.37c 10.17 ± 1.00b,c,d 注:F组间= 140.736,P < 0.01;F时间= 78.134,P < 0.01;a与平行对照组相比,P < 0.05;b与3 d时相比,P < 0.05;c与7 d时相比,P < 0.05;d与14 d时相比,P < 0.05。 -
[1] 陈涛, 冯高科, 易欣, 等.成体干细胞治疗皮肤损伤性疾病的研究进展[J].广西医学, 2019, 41(19):2478-2481. http://www.wanfangdata.com.cn/details/detail.do?_type=perio&id=gxyx201919015 [2] 李婷, 陈莉智, 黄文华.骨髓间充质干细胞在基础医学及临床应用中的研究进展[J].中国医学物理学杂志, 2019, 36(8):962-967. http://www.wanfangdata.com.cn/details/detail.do?_type=perio&id=zgyxwlxzz201908019 [3] 薛碧宇, 薛斌. BMSC共培养对人瘢痕疙瘩成纤维细胞DNMT1的影响[J].中国细胞生物学学报, 2019, 41(8):1517-1522. http://www.wanfangdata.com.cn/details/detail.do?_type=perio&id=xbswxzz201908005 [4] LI Q, ZHANG C, FU X. Will stem cells bring hope to pathological skin scar treatment?[J]. Cytotherapy, 2016, 18(8):943-956. doi: 10.1016/j.jcyt.2016.05.008
[5] ZHENG K, WU W, YANG S, et al. Bone marrow mesenchymal stem cell implantation for the treatment of radioactivityinduced acute skin damage in rats[J]. Mol Med Rep, 2015, 12(5):7065-7071. doi: 10.3892/mmr.2015.4270
[6] WANG J, LIU S, LI J, et al. Roles for miRNAs in osteogenic differentiation of bone marrow mesenchymal stem cells[J]. Stem Cell Res Ther, 2019, 10(1):197. doi: 10.1186/s13287-019-1309-7
[7] ZHANG J, LA X, FAN L, et al. Immunosuppressive effects of mesenchymal stem cell transplantation in rat burn models[J]. Int J Clin Exp Pathol, 2015, 8(5):5129-5136. http://pubmedcentralcanada.ca/pmcc/articles/PMC4503080/
[8] GUO X, XIA B, LU XB, et al. Grafting of mesenchymal stem cell-seeded small intestinal submucosa to repair the deep partial-thickness burns[J]. Connect Tissue Res, 2016, 57(5):388-397. doi: 10.1080/03008207.2016.1193173
[9] 崔玉芳, 夏国伟, 付小兵, 等.肥大细胞在单纯和放射复合伤口愈合中的作用[J].中国病理生理杂志, 2002, 18(5):11-14. http://www.wanfangdata.com.cn/details/detail.do?_type=perio&id=zgblslzz200205003 [10] 马晓菁, 谢东珊, 张娇, 等.大鼠骨髓间充质干细胞在创面愈合中的作用[J].中国组织工程研究与临床康复, 2009, 13(32):6299-6302. http://www.wanfangdata.com.cn/details/detail.do?_type=perio&id=xdkf200932024 [11] HE Y, CHEN D, YANG L, et al. The therapeutic potential of bone marrow mesenchymal stem cells in premature ovarian failure[J]. Stem Cell Res Ther, 2018, 9(1):263. doi: 10.1186/s13287-018-1008-9
[12] 马嵋, 张燕, 魏琴, 等.骨髓间充质干细胞对仓鼠皮肤深Ⅱ度烫伤的治疗作用及机制研究[J].实验动物与比较医学, 2012, 32(6):499-502. http://www.wanfangdata.com.cn/details/detail.do?_type=perio&id=shsydwkx201206009 -
期刊类型引用(0)
其他类型引用(1)





 下载:
下载: