Role of NOX4 and NF-κB in oxidative stress of HepG2 cells induced by sodium fluoride
-
+ English摘要:目的
研究NOX4、NF-κB在氟化钠诱导HepG2细胞氧化应激中的作用。
方法分别用浓度为0、10、20、40、80 mg/L的氟化钠处理细胞24 h,采用硫代巴比妥酸法测定细胞内丙二醛(malondialdehyde,MDA)含量,羟胺法测定细胞内总超氧化物歧化酶(superoxide dismutase,SOD)活力。免疫印迹法检测细胞内细胞核因子p65磷酸化水平和还原型烟酰胺腺嘌呤二核苷酸磷酸氧化酶4(nicotinamide adenine dinucleotide phosphate oxidase 4,NOX4)蛋白表达水平;用NOX4抑制剂夹竹桃麻素(apocynin)预处理30 min后,再用40 mg/L氟化钠处理24 h,免疫印迹法检测细胞内p65磷酸化水平和NOX4蛋白表达水平反映HepG2细胞内的氧化应激状况。
结果经氟化钠处理后,20、40、80 mg/L剂量组HepG2细胞内的MDA含量较对照组相比明显升高(P < 0.01),各剂量组细胞内总SOD活力均较对照组明显降低(P < 0.01),40、80 mg/L剂量组NOX4蛋白表达水平和20、40、80 mg/L剂量组p65蛋白磷酸化水平均较对照组升高(P < 0.01或0.05),存在着剂量效应;与单纯使用氟化钠处理组相比,用apocynin预处理细胞后,40 mg/L氟化钠诱导细胞内p65磷酸化水平和NOX4蛋白表达水平皆降低(P < 0.05或0.01)。
结论氟化钠诱导HepG2细胞产生氧化应激可能与激活NF-κB/NOX4途径有关。
-
关键词:
- 氟化钠 /
- 氧化应激 /
- HepG2细胞 /
- 还原烟酰胺腺嘌呤二核苷酸磷酸氧化酶4 /
- 核因子κB
-
地方性氟中毒已成为威胁人类健康的全球性公共卫生问题,过量的氟摄入除了会引起氟斑牙和氟骨病外,也会累及肾脏、肝脏等其他器官。肝脏是人体最重要的解毒器官,也是很多毒物作用的靶器官[1-4]。有研究表明氟对肝脏的损伤可能与氟诱导肝细胞产生氧化应激有关,氧化自由基引起生物膜氧化,改变生物膜流动性和完整性,最终导致细胞结构和功能紊乱,继而引起细胞损伤[5-7]。但其中涉及的机制和相关亚细胞结构尚不清楚。NAPDH氧化酶家族是产生活性氧(reactive oxygen species,ROS)的关键酶,还原烟酰胺腺嘌呤二核苷酸磷酸氧化酶4(nicotinamide adenine dinucleotide phosphate reduced oxidase 4,NOX4)在肝脏细胞中表达,前期研究发现一些疾病伴随的氧化应激损伤与NOX4密切相关[8-11]。核因子κB(nuclear factor kappa-B,NF-κB)是广泛存在于细胞内的一种核转录因子,它的激活与细胞凋亡和氧化应激的发生密切相关,并起着重要的生物学效应[12-13]。本研究拟观察NOX4、NF-κB在氟化钠诱导HepG2细胞氧化应激中的作用,为职业性氟中毒和地方性氟中毒的防控和治疗提供基础理论依据。
1. 材料与方法
1.1 主要仪器与试剂
二氧化碳细胞培养箱(松下MCO-18AC)、高速低温离心机(湘鹰TGL-24M)、超净工作台(苏净安泰SW-CJ-2FD)、超声细胞裂解仪(信仪ⅡD)、超低温冰箱(三洋MDF-382E)、化学发光成像仪(天能5200)、酶标仪(Biotek EPOCH2);氟化钠(优级纯)购自于国药集团;高糖DMEM培养基、细胞培养双抗均购于Hyclone公司;优级胎牛血清购于杭州四季青生物科技有限公司;丙二醛(malonic dialdehyde,MDA)和超氧化物歧化酶(superoxide dismutase,SOD)测定试剂盒购于南京建成生物科技有限公司;增强型ECL发光液购于武汉塞维尔生物科技有限公司;辣根过氧化酶标记二抗购于北京中杉金桥生物科技有限公司;NOX4抗体购于Lifespan公司;p-p65、p65、GAPDH抗体均购Cell Signing Technology公司,CCK-8试剂盒购于碧云天生物科技有限公司,apocynin和二甲基亚砜均购于Sigma公司。
HepG2细胞由安徽医科大学第一附属医院孔德润教授惠赠,复苏后用含体积分数10%胎牛血清、1%双抗的DMEM培养基在37 ℃、体积分数5%CO2饱和湿度下培养。
1.2 方法
1.2.1 CCK-8测定HepG2细胞活性
将细胞置于96孔板中,每组细胞设置3个复孔,用不同浓度氟化钠处理24 h后,每孔加入CCK-8工作液10 μL,37 ℃孵育2 h,用Biotek EPOCH2酶标仪测定450 nm波长下的吸光度值。活细胞数量与450 nm下吸光度值呈正相关。
1.2.2 细胞处理与分组
待细胞长至90%密度时传代至25 cm2的培养瓶,待细胞长至80%密度时,吸去培养基,用磷酸盐缓冲液(phosphate buffered saline,PBS)漂洗1次,换含3%胎牛血清的培养基,各瓶细胞加入氟化钠溶液,使培养瓶中氟化钠终浓度分别为0、10、20、40、80 mg/L,每组细胞设置3个复孔,继续培养24 h;用100 μmol/L浓度的apocynin预处理细胞30 min,再用40 mg/L氟化钠处理细胞24 h。
1.2.3 细胞内MDA含量和总SOD活力测定
弃去培养上清液,用PBS漂洗3遍,每个培养瓶加入600 μL生理盐水,用细胞刮刀刮下细胞,移入1.5 mL EP管中,冰上超声裂解2 min,4 ℃下以12 000 r/min(离心半径5 cm)离心5 min,取上清液测定MDA含量和总SOD活力,测定过程严格按照试剂盒操作说明进行。
1.2.4 细胞中氧化应激相关蛋白磷酸化水平和表达水平的测定
应用Western blot检测细胞中氧化应激相关指标。每组细胞设置3个复孔,细胞加药处理24 h后,用PBS漂洗2次,每瓶细胞加400 μL裂解液,冰上裂解10 min,以13 000 r/min(离心半径5 cm)离心10 min,取上清液,加入上样缓冲液,100 ℃变性8 min。经12.5%(质量分数)十二烷基硫酸钠聚丙烯酰胺凝胶电泳后,湿转至PVDF膜上,在5%(质量分数)脱脂牛奶中室温封闭1 h。在NOX4(1:4 000)、p-p65(1:2 000)、p65(1:2 000)、GAPDH(1:10 000)一抗中4 ℃孵育过夜,用PBST洗膜4次,每次5 min,然后用HRP标记的二抗(1:5 000)中室温孵育1.5 h,PBST洗膜3次,每次5 min,再用PBS洗膜5 min,放入ECL发光液中孵育1 min,用Tanon-5200化学发光成像仪拍摄成像。
1.2.5 质量控制措施
为了减少实验过程中的偶尔误差,一般细胞实验我们至少设置3个复孔。本研究中检测细胞活性、细胞中MDA含量和SOD活力的实验操作均严格按照操作说明进行,每个样品进行2次检测,取2次检测的均值进行分析。
1.2.6 统计学分析
Western blot结果图像用Image J软件进行灰度分析,采用SPSS 19.0软件对实验数据进行分析。定量资料以均数±标准差(x ± s)表示,多组间比较采用ANOVA方差分析,多组间两两比较采用SNK法。检验水准α = 0.05。
2. 结果
2.1 不同浓度氟化钠对HepG2细胞活性的影响。
经氟化钠处理24 h后,各浓度组细胞活性差异无统计学意义(P > 0.05),见表 1。
表 1 不同浓度氟化钠处理24 h后各组细胞450 nm下吸光度值组别 样品数 吸光度 对照组 3 0.392 ± 0.005 氟化钠10 mg/L组 3 0.368 ± 0.016 氟化钠20 mg/L组 3 0.356 ± 0.023 氟化钠40 mg/L组 3 0.342 ± 0.027 氟化钠80 mg/L组 3 0.355 ± 0.031 F值 2.12 P值 >0.05 2.2 氟化钠对HepG2细胞内MDA和总SOD的影响
经氟化钠处理24 h后,细胞内MDA含量较对照组明显增加(P < 0.01),氟化钠20、40、80 mg/L组MDA含量均高于对照组(P < 0.01),且存在着剂量-效应关系,细胞内总SOD活力较对照组明显降低(P < 0.01),各剂量组总SOD活力均低于对照组(P < 0.05或0.01),也存在着剂量-效应关系。见表 2。
表 2 不同浓度氟化钠处理24 h后各组细胞内MDA含量和总SOD活力组别 样品数 MDA /(nmol/mg) SOD /(U/mg) 对照组 3 10.16 ± 0.77 42.76 ± 2.34 氟化钠10 mg/L组 3 12.08 ± 1.05 35.95 ± 2.28b 氟化钠20 mg/L组 3 13.48 ± 0.81 a 31.40 ± 1.67 a 氟化钠40 mg/L组 3 17.92 ± 1.36 a 23.28 ± 2.32 a 氟化钠80 mg/L组 3 23.30 ± 2.28 a 22.58 ± 3.61 a F值 42.14 34.50 P值 < 0.01 < 0.01 注:与对照组比较,a P < 0.01。 2.3 氟化钠对HepG2细胞内NOX4蛋白表达水平和p65磷酸化水平的影响
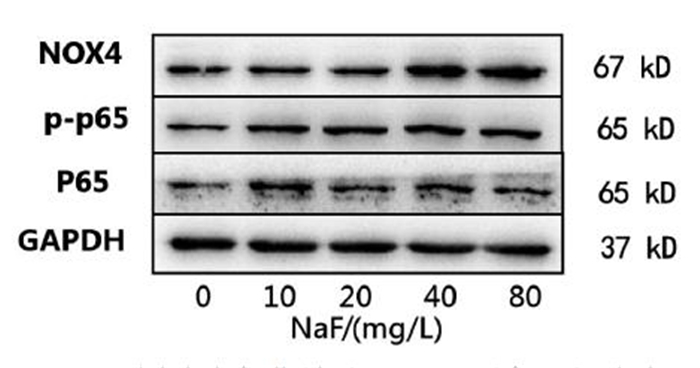
经氟化钠处理24 h后,细胞内NOX4蛋白表达水平升高,其中氟化钠40、80 mg/L组高于对照组(P < 0.01);p65磷酸化水平较对照组升高,其中氟化钠20、40、80 mg/L组高于对照组(P < 0.05或0.01)。见图 1、表 3。
表 3 不同浓度氟化钠处理24 h后各组细胞内NOX4蛋白表达水平和p65磷酸化水平组别 样品数 NOX4/GAPDH p-p65/p65 对照组 3 1.00 ± 0.18 1.00 ± 0.10 氟化钠10 mg/L组 3 1.09 ± 0.07 1.10 ± 0.16 氟化钠20 mg/L组 3 1.23 ± 0.15 1.62 ± 0.07 b 氟化钠40 mg/L组 3 2.94 ± 0.51 a 1.94 ± 0.12 b 氟化钠80 mg/L组 3 3.38 ± 0.44 a 2.09 ± 0.19 b F值 40.39 43.16 P值 < 0.01 < 0.01 注:与对照组比较,a P < 0.01,b P < 0.05。 2.4 apocynin预处理后细胞内NOX4蛋白表达水平和p65磷酸化水平
用apocynin预处理后,再用氟化钠处理细胞24 h,细胞内NOX4蛋白表达水平和p65磷酸化水平较氟化钠处理组降低,差异有统计学意义(P < 0.01)。见图 2、表 4。
表 4 用apocynin预处理再用氟化钠处理24 h后各组细胞内NOX4蛋白表达水平和p65磷酸化水平组别 样品数 NOX4/GHAPDH p-p65/p65 对照组 3 1.00 ± 0.19 1.00 ± 0.08 NaF处理组 3 2.56 ± 0.30 a 2.23 ± 0.15 a apocynin处理组 3 0.96 ± 0.08 1.06 ± 0.15 NaF+apocynin处理组 3 1.48 ± 0.09 b 1.43 ± 0.17 b F值 63.02 47.54 P值 < 0.01 < 0.01 3. 讨论
前期研究表明氟引起肝脏的损伤可能与肝脏内氧化应激有关,过量氟的摄入导致肝细胞内脂质过氧化发生,同时改变细胞内氧化-抗氧化对比,打破这种平衡继而引发细胞损伤[5-6]。本次研究结果表明:与对照组相比,20 mg/L浓度的氟化钠处理会引起HepG2细胞内丙二醛浓度升高(P < 0.01),10 mg/L浓度的氟化钠处理会降低HepG2细胞内总超氧化物歧化物酶的活性(P < 0.05),这与先前氟损伤的自由基说是一致的。
NOX4作为产生ROS的关键酶参与了细胞内氧化应激的发生,但是氟对肝细胞损伤与NOX4关系的研究尚未有报道,本研究结果显示:与对照组相比,40 mg/L氟化钠处理会明显上调HepG2细胞内NOX4蛋白表达水平(P < 0.01),这提示经氟处理后细胞内ROS含量可能升高,细胞处于氧化应激状态,高浓度的ROS又会作用于细胞内的脂质大分子及核酸,引发脂质过氧化,损伤细胞正常的结构和功能。细胞内脂质过氧化标志丙二醛浓度的升高和抗氧化物酶活力降低也支持了蛋白检测的结果。
NF-κB是广泛存在于细胞内的一种具有多向调节核转录因子,它参与调控细胞氧化应激的发生过程。其中p65是NF-κB磷酸化中最重要的一个亚基[14]。本研究结果显示:与对照组相比,20 mg/L氟化钠处理会增加p65的磷酸化水平(P < 0.05),使用NADPH氧化酶抑制剂apocynin预处理细胞后可明显下调NOX4蛋白表达水平以及p65的磷酸化水平,减轻细胞内氧化应激水平。由此可见,氟化钠诱导HepG2细胞氧化应激可能与NF-κB通路激活以及NOX4蛋白表达上调有关。本研究使用HepG2细胞作为氧化应激细胞模型,HepG2细胞作为肝癌细胞系,其生物学特性与正常的肝细胞存在一定差异;在本研究中每组样本量只有3个,这也增大了实验结果存在偶然误差的可能,这是本研究的局限性。氧化应激是一个复杂的应激过程,其发生还可能与PI3K/AKT、AMPK、Nrf2等通路的激活有关[15],本研究仅证实氟化钠诱导HepG2细胞氧化应激与NF-κB/NOX4途径激活有关,且单纯的体外细胞实验结果不能完全类推到体内实验结果,因此涉及的其他途径以及机制尚待进一步动物体内实验去证实。
作者声明 本文无实际或潜在的利益冲突 -
表 1 不同浓度氟化钠处理24 h后各组细胞450 nm下吸光度值
组别 样品数 吸光度 对照组 3 0.392 ± 0.005 氟化钠10 mg/L组 3 0.368 ± 0.016 氟化钠20 mg/L组 3 0.356 ± 0.023 氟化钠40 mg/L组 3 0.342 ± 0.027 氟化钠80 mg/L组 3 0.355 ± 0.031 F值 2.12 P值 >0.05 表 2 不同浓度氟化钠处理24 h后各组细胞内MDA含量和总SOD活力
组别 样品数 MDA /(nmol/mg) SOD /(U/mg) 对照组 3 10.16 ± 0.77 42.76 ± 2.34 氟化钠10 mg/L组 3 12.08 ± 1.05 35.95 ± 2.28b 氟化钠20 mg/L组 3 13.48 ± 0.81 a 31.40 ± 1.67 a 氟化钠40 mg/L组 3 17.92 ± 1.36 a 23.28 ± 2.32 a 氟化钠80 mg/L组 3 23.30 ± 2.28 a 22.58 ± 3.61 a F值 42.14 34.50 P值 < 0.01 < 0.01 注:与对照组比较,a P < 0.01。 表 3 不同浓度氟化钠处理24 h后各组细胞内NOX4蛋白表达水平和p65磷酸化水平
组别 样品数 NOX4/GAPDH p-p65/p65 对照组 3 1.00 ± 0.18 1.00 ± 0.10 氟化钠10 mg/L组 3 1.09 ± 0.07 1.10 ± 0.16 氟化钠20 mg/L组 3 1.23 ± 0.15 1.62 ± 0.07 b 氟化钠40 mg/L组 3 2.94 ± 0.51 a 1.94 ± 0.12 b 氟化钠80 mg/L组 3 3.38 ± 0.44 a 2.09 ± 0.19 b F值 40.39 43.16 P值 < 0.01 < 0.01 注:与对照组比较,a P < 0.01,b P < 0.05。 表 4 用apocynin预处理再用氟化钠处理24 h后各组细胞内NOX4蛋白表达水平和p65磷酸化水平
组别 样品数 NOX4/GHAPDH p-p65/p65 对照组 3 1.00 ± 0.19 1.00 ± 0.08 NaF处理组 3 2.56 ± 0.30 a 2.23 ± 0.15 a apocynin处理组 3 0.96 ± 0.08 1.06 ± 0.15 NaF+apocynin处理组 3 1.48 ± 0.09 b 1.43 ± 0.17 b F值 63.02 47.54 P值 < 0.01 < 0.01 -
[1] 陶欣, 于燕妮, 朱志坚, 等.慢性氟中毒对大鼠肝脏Notch1、Hes1蛋白表达影响[J].中国公共卫生, 2015, 31(6):747-750. https://www.cnki.com.cn/Article/CJFDTOTAL-ZGGW201506015.htm [2] INKIELEWICZ-STEPNIAK I. Impact of fluoxetine on liver damage in rats[J]. Pharmacol Rep, 2011, 63(2):441-447. doi: 10.1016/S1734-1140(11)70510-2
[3] NIU Q, HE P, XU S, et al. Fluoride-induced iron overload contributes to hepatic oxidative damage in mouse and the protective role of Grape seed proanthocyanidin extract[J]. J Toxicol Sci, 2018, 43(5):311-319. doi: 10.2131/jts.43.311
[4] WEI W, PANG S. The pathogenesis of endemic fluorosis:research progress in the last 5 years[J]. J Cell Mol Med, 2019, 23(4):2333-2342. doi: 10.1111/jcmm.14185
[5] HASSAN H A. Mitigating effects of antioxidant properties of black berry juice on sodium fluoride induced hepatotoxicity and oxidative stress in rats[J]. Food Chem Toxicol, 2009, 47(9):2332-2337. doi: 10.1016/j.fct.2009.06.023
[6] 官志忠.氧化应激在地方性氟中毒分子发病机制中的作用[J].中华地方病学杂志, 2016, 35(2):79-82. doi: 10.3760/cma.j.issn.2095-4255.2016.02.001 [7] 董阳婷, 王娅, 魏娜, 等.慢性氟中毒大鼠大脑和血清氧化应激水平改变及维生素E的拮抗作用[J].中华地方病学杂志, 2016, 35(3):178-181. doi: 10.3760/cma.j.issn.2095-4255.2016.03.006 [8] 杨成伟, 王取南, 陈可洋.瘦素改善2型糖尿病ob/ob小鼠糖和脂质代谢作用机制的探讨[J].中华疾病控制杂志, 2016, 20(9):940-944. https://www.cnki.com.cn/Article/CJFDTOTAL-JBKZ201609020.htm [9] BETTAIEB A, JIANG J X, SASAKI Y, et al. Hepatocyte nicotinamide adenine dinucleotide phosphate reduced oxidase 4 regulates stress signaling, fibrosis, and insulin sensitivity during development of steatohepatitis in mice[J]. Gastroenterology, 2015, 149(2):468-480.e10. doi: 10.1053/j.gastro.2015.04.009
[10] TARAFDAR A. The role of NADPH oxidases and oxidative stress in neurodegenerative disorders[J]. Int J Mol Sci, 2018, 19(12):3824. doi: 10.3390/ijms19123824
[11] DREVET S, GAVAZZI G, GRANGE L, et al. Reactive oxygen species and NADPH oxidase 4 involvement in osteoarthritis[J]. Exp Gerontol, 2018, 111:107-117. doi: 10.1016/j.exger.2018.07.007
[12] WANG Y, TAO J, JIANG M, et al. Apocynin ameliorates diabetic retinopathy in rats:involvement of TLR4/NF-κB signaling pathway[J]. Int Immunopharmacol, 2019, 73:49-56. doi: 10.1016/j.intimp.2019.04.062
[13] MOLDOGAZIEVA N T, MOKHOSOEV I M, FELDMAN N B, et al. ROS and RNS signalling:adaptive redox switches through oxidative/nitrosative protein modifications[J]. Free Radic Res, 2018, 52(5):507-543. doi: 10.1080/10715762.2018.1457217
[14] 李丽, 陈玉婷, 曾希. RelA/p65的磷酸化调节及其与肿瘤的关系[J].中南医学科学杂志, 2018, 46(2):216-220. https://www.cnki.com.cn/Article/CJFDTOTAL-HYYY201802029.htm [15] 陈晨, 殷园园, 武夏芳, 等.活性氧通过MAPKs和PI3K/AKT通路激活Nrf2研究进展[J].中国公共卫生, 2016, 32(6):870-873. https://www.cnki.com.cn/Article/CJFDTOTAL-ZGGW201606041.htm -
期刊类型引用(3)
1. 吴晓军,谢石荣,温建平,干红芳,曾金水. 厦门市海沧区制造业职业病危害现状调查. 职业与健康. 2025(02): 145-149+155 .  百度学术
百度学术
2. 郑晋南,张思雨,余悦,胡伟江. 2020-2021年全国非金属矿物制品业企业粉尘及噪声监测结果分析. 工业卫生与职业病. 2024(04): 308-312 .  百度学术
百度学术
3. 苗芝秋. 职业病防治的问题及解决策略分析. 中国卫生产业. 2024(06): 231-233+237 .  百度学术
百度学术
其他类型引用(0)





 下载:
下载: