Study on toxicokinetics of paraquat by gavage in rabbits
-
+ English摘要:目的 探讨经口染毒百草枯在家兔体内的毒物代谢动力学过程。方法 分别以100 mg/kg和200 mg/kg的剂量给家兔灌胃染毒,于染毒后不同时间采集血液样本,应用液相色谱质谱法测定各样本中百草枯的含量,绘制浓度-时间曲线,并用DAS 3.0软件计算毒物代谢动力学参数。结果 以100 mg/kg剂量的百草枯(质量分数20%)经口染毒后(1.96 ± 2.41)h,家兔体内血液中百草枯浓度达到峰值,之后血药浓度迅速下降,非房室模型统计矩参数中峰质量浓度为(2.53 ± 0.84)mg/L、半衰期为(8.41 ± 1.89)h、浓度曲线下面积为(14.10 ± 3.21)mg/(L·h)。200 mg/kg百草枯经口染毒后(1.76 ± 1.10)h达峰,之后血药浓度迅速下降,非房室模型统计矩参数中峰浓度为(9.21 ± 4.43)mg/L、半衰期为(15.47 ± 12.11)h、浓度曲线下面积为(76.05 ± 34.30)mg/(L·h)。两组家兔血浆中百草枯达峰时间和平均留存时间的差异无统计学意义(P > 0.05)。结论 百草枯经口染毒在家兔体内的变化过程符合三室模型特征,获得了不同染毒剂量百草枯在家兔体内的毒物代谢动力学参数。
-
百草枯(paraquat,PQ)是一种非选择性触杀除草剂,由于除草效率高,接触土壤后又可钝化失活,不会伤害植物根系,也不会造成环境污染,使得PQ曾在全球120多个国家和地区广泛使用。然而,随着PQ使用量的增加,也出现了大量PQ中毒事故[1],2008—2011年间,国家中毒控制中心中毒咨询热线确认的PQ中毒病例达824例,其中大多数为口服PQ中毒,病死率高达31.0% ~ 97.0% [2]。为此我国自2014年7月1日起,撤销了PQ水剂登记和生产许可,停止其生产[3]。但目前仍有大量库存在市场流通和使用,甚至有不法商贩将PQ冠以“敌草快”“草铵膦”等低毒除草剂出售和使用,造成的中毒事件仍层出不穷[4-5]。本研究建立了家兔经口染毒PQ的实验动物模型,并研究PQ在兔体内的毒物代谢动力学(toxicokinetics,TK)过程,以期为PQ中毒的诊断和治疗提供依据。
1. 材料与方法
1.1 材料
1.1.1 实验动物
14只普通级新西兰白色家兔购自广东省医学实验动物中心,雌雄各半,体质量(2.22 ± 0.20)kg,实验动物合格证号:SCXK(粤)2019-0035。饲养于深圳市疾病预防控制中心动物房。按照GB 14925—2010《实验动物环境及设施》 [6]的条件进行常规饲养,动物自由采食和饮水。本研究通过深圳市职业病防治院伦理委员会伦理审查。
1.1.2 仪器和试剂
Shimadzu LC-20ADXR高效液相色谱仪(日本岛津公司)、API 4000+三重四级杆串联质谱仪(美国AB Sciex公司)、SIGMA 3K15高速冷冻离心机(德国SIGMA公司)、MS3型漩涡混合器(德国IKA公司);XBridge BEH-HILIC色谱柱(美国Waters公司)、PQ水剂(质量分数20%)(江苏南通先正达公司)、PQ标准品(上海安谱公司)、PQ-d8标准品(北京曼哈格生物科技有限公司);乙腈、甲醇、甲酸铵(均为色谱纯,中国CNW公司)。
1.2 方法
1.2.1 动物分组与染毒
家兔在动物房适应性喂养7 d后,按照随机数字表法分为低剂量染毒组(6只)和高剂量染毒组(8只)2组。家兔染毒前24 h禁食,染毒前12 h禁水。实验前将家兔固定于家兔固定架上,以婴儿导尿管为胃管,经开口器中间孔插入约25 ~ 30 cm,进入胃内后再次用10 mL注射器进行抽吸,确认插入位置正确后进行灌胃染毒操作。低剂量染毒组:以每千克体重2 mL体积的50 mg/mL PQ水溶液灌胃,即染毒剂量为100 mg/kg,一次性灌胃染毒。高剂量染毒组:以每千克体重2 mL体积的100 mg/mL PQ水溶液灌胃,即染毒剂量为200 mg/kg,一次性灌胃染毒。染毒后4 h恢复饮水,8 h恢复进食。
1.2.2 样品采集
两组家兔分别在染毒前(0 min)和染毒后10 min、20 min、40 min、1 h、2 h、3 h、4 h、8 h、24 h、72 h和7 d经耳中央动脉采集血液0.5 ~ 1.0 mL,置于肝素抗凝管中,然后立即在4 ℃低温,4 000 r/min(离心半径16.9 cm)离心出血浆用于PQ检测。
1.2.3 血浆中PQ检测
(1)样品前处理。取200 μL血浆样品于1.5 mL塑料离心管中,加入800 μL乙腈甲酸水溶液(乙腈∶体积分数0.1%的甲酸水溶液= 3 ∶ 1),加入40 μL 1.0 mg/L PQ-d8内标液,涡旋振荡5 min,12 000 r/min(离心半径8.26 cm)离心5 min,取上清液400 μL至塑料进样瓶,用HPLC-MS/MS进行质谱分析。若5倍稀释样品的PQ浓度超过测定的线性范围(0.1 mg/L),则采用乙腈甲酸水溶液10倍、20倍、50倍、100倍或200倍稀释血浆样品后进行分析。
(2)液相色谱条件。色谱柱:XBridge BEH-HILIC(100 mm × 2.1 mm × 2.5 μm),保护柱(5 mm × 2.1 mm × 2.5 μm);流动相:乙腈∶(100 mmol/L甲酸铵+ 体积分数0.5%甲酸水溶液)= 60∶40,等度洗脱;柱温:30 ℃;进样体积:2 μL。
(3)质谱条件。离子化模式:电喷雾电离正离子模式(ESI +);质谱扫描方式:多反应监测;碰撞气:12 psi(1 psi = 6 894.757 Pa);气帘气:35 psi;离子喷雾电压:5 000 V;雾化干燥气温度:650 ℃,雾化气:50 psi,辅助气:55 psi;射入电压:10 V;碰撞室射出电压:13 V。PQ及内标物的多反应监测条件见表 1。
表 1 PQ及内标物的多反应监测条件化合物 母离子m/z 子离子m/z 去簇电压/v 碰撞能量/ eV PQ 171.2 155.2 85 40 77.2 85 52 PQ-d8 179.2 162.2 85 43 82.2 85 52 1.2.4 毒物代谢动力学参数计算
将各时点的PQ血浆浓度录入Data Analysis System 3.0(DAS 3.0)软件,计算房室模型和非房室模型统计矩毒物代谢动力学参数,包括:血药浓度时间曲线下面积(area under curve,AUC)、血药浓度一阶矩时间曲线下面积(first moment area under the curve,AUMC)、平均滞留时间(mean residence time,MRT)、达峰时间(peak time,Tmax)、峰浓度(peak concentration,Cmax)、平均滞留时间方差(variance of mean residence time,VRT)、尾段斜率(elimination rate constant,λz)、尾点血药浓度(last blood concentration,Clast)、半衰期(half life,t1/2)等。
1.2.5 统计学分析
实验数据使用Excel软件进行管理,计量资料结果以均数±标准差(x ± s)的形式描述。应用SPSS 18.0软件对两组动物在观察期间的TK参数进行独立样本t检验,以P < 0.05为差异有统计学意义。
2. 结果
2.1 基本情况
低剂量染毒组的家兔未出现明显中毒症状,高剂量染毒组中2只家兔在染毒后约24 h出现行动缓慢,拒绝饮水和进食,同组其余动物未观察到异常反应。2只出现中毒症状的实验动物分别于染毒后30 h和75 h死亡,后述TK结果均已剔除死亡动物的数据。
2.2 血浆中PQ的检测方法
PQ在10.0 ~ 120.0 μg/L质量浓度范围内线性良好,回归方程:y = 0.053 1 x - 0.020 0;相关系数为0.998 5,PQ在血浆中最低检出限为1.98 μg/L,样品加标回收率在100.2% ~ 106.9%之间,相对标准偏差在2.1% ~ 3.3%之间。
2.3 家兔血浆PQ的浓度-时间曲线
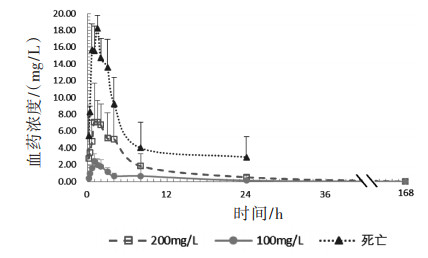
一次性经口染毒后,PQ通过消化道迅速吸收入血,染毒后10 min即可在血浆中检出PQ。低剂量染毒组达峰时间在60 min左右,峰浓度为2.5 mg/L,然后随时间推移迅速降低,在8 h时已降至较低水平,至24 h基本消除。高剂量染毒组的动物血浆PQ浓度在60 ~ 90 min期间达峰,峰浓度为7.3 mg/L,随后逐渐下降,在3 ~ 4 h期间PQ浓度出现持续1 h左右的平台期,随后快速下降,至24 h后达到较低水平,72 h后基本消除。由浓度-时间曲线图可以看出,染毒剂量与血中PQ浓度并非简单线性关系,而是表现为染毒剂量越高,吸收比例越高的趋势。实验期间死亡的2只动物各时点血中PQ浓度均高于同等剂量染毒未死亡的动物。见图 1。
2.4 代谢动力学参数
家兔经口染毒PQ的房室模型呈三室模型分布,房室模型TK参数见表 2,非房室模型统计矩TK参数见表 3。以200 mg/kg的剂量染毒时,相比100 mg/kg PQ染毒,AUC更大、峰浓度更高,差别有统计学意义(P < 0.05)。两组家兔血浆中PQ达峰时间和平均留存时间差异无统计学意义(P > 0.05)。
表 2 PQ的毒物代谢动力学房室模型参数参数 单位 染毒剂量/(mg/kg) t值 P值 100 200 AUC(0 ~ t) mg/(L·h) 19.23 ± 14.21 63.54 ± 42.56 - 2.419 0.036 AUC(0 ~ ∞) mg/(L·h) 19.75 ± 14.23 65.00 ± 42.81 - 2.457 0.034 t1/2α h 1.09 ± 1.86 1 156.13 ± 2 829.33 - 1.000 0.363 t1/2β h 2 424.76 ± 3 500.85 4 631.29 ± 3 563.47 - 1.082 0.305 t1/2γ h 5.50 ± 4.14 -4 168.55 ± 10 222.88 1.000 0.363 V1 L/kg 1 488.04 ± 2 382.90 641.41 ± 1 167.72 0.779 0.454 V2 L/kg (-8.40 ± 20.59)× 108 (-1.09 ± 2.68)×107 - 0.987 0.369 V3 L/kg (8.55 ± 20.95)× 108 (2.05 ± 6.60)×106 0.998 0.364 CL1 L/(h·kg) 2 312.44 ± 3 900.34 1 359.86 ± 2 477.70 0.505 0.625 CL2 L/(h·kg) (-3.46 ± 8.46)× 106 -1 345.81 ± 3 212.53 - 1.000 0.363 CL3 L/(h·kg) (3.45 ± 8.46)×106 301.51 ± 628.66 1.000 0.363 K10 1/h 1.28 ± 0.41 59.81 ± 145.44 - 0.986 0.369 K12 1/h -621.15 ± 1 526.27 -76.03 ± 180.97 - 0.869 0.405 K21 1/h 1.77 ± 2.46 0.07 ± 0.08 1.695 0.151 K31 1/h 0.07 ± 0.09 0.01 ± 0.01 1.865 0.120 K13 1/h 622.96 ± 1 525.13 17.79 ± 35.33 0.972 0.376 Ka 1/h 2.44 ± 2.06 1.72 ± 1.47 0.704 0.498 t1/2ka 1/h 0.90 ± 1.37 0.75 ± 0.70 0.230 0.823 Tmax h 1.96 ± 2.41 1.76 ± 1.10 0.181 0.860 Cmax mg/L 2.37 ± 0.82 7.56 ± 3.14 - 3.918 0.009* 注:AUC:血药浓度-时间曲线下面积;t1/2α:中央室半衰期;t1/2β:第一周边室半衰期;t1/2γ:第二周边室半衰期(消除半衰期);V1:中央室表观分布容积;V2:第一周边室表观分布容积;V3:第二周边室表观分布容积;CL1:中央室清除率;CL2:第一周边室清除率;CL3:第二周边室清除率;K:速率常数;Ka:吸收速率常数;t1/2ka:吸收半衰期;Cmax:峰浓度;Tmax:达峰时间。 表 3 PQ的毒物代谢动力学非房室模型统计矩参数参数 单位 染毒剂量/(mg/kg) t值 P值 100 200 AUC(0~t) mg/(L·h) 14.06 ± 3.19 72.89 ± 35.15 - 4.083 0.009 AUC(0~∞) mg/(L·h) 14.10 ± 3.21 76.05 ± 34.30 - 4.404 0.007 AUMC(0~t) h2·mg/L 171.50 ± 88.72 993.68 ± 325.32 - 5.972 0.009 AUMC(0~∞) h2·mg/L 175.02 ± 92.99 1356.91 ± 585.59 - 4.883 0.004 MRT(0~t) h 12.09 ± 5.14 14.43 ± 3.17 0.900 0.365 MRT(0~∞) h 12.28 ± 5.23 19.03 ± 8.42 - 1.659 0.128 VRT(0~t) h2 217.79 ± 210.42 340.65 ± 145.82 - 1.175 0.267 VRT(0~∞) h2 230.72 ± 222.02 813.79 ± 771.92 - 1.778 0.127 λz 1/h 0.08 ± 0.01 0.07 ± 0.04 0.717 0.500 t1/2z h 8.41 ± 1.89 15.47 ± 12.11 - 1.140 0.215 Tmax h 1.33 ± 0.41 2.16 ± 1.47 - 1.336 0.232 Vz L/kg 89.88 ± 26.04 67.36 ± 55.40 0.902 0.388 CLz L/(h·kg) 7.49 ± 2.19 2.98 ± 0.99 4.600 0.001 Cmax mg/L 2.53 ± 0.84 9.21 ± 4.43 - 3.629 0.013 Clast mg/L 0.002 ± 0.003 0.07 ± 0.09 - 1.910 0.114 注:AUC:血药浓度-时间曲线下面积;AUMC:血药浓度一阶矩时间曲线下面积;MRT:平均滞留时间;VRT:平均滞留时间方差;λz:尾点斜率;t1/2z:统计矩计算的半衰期;Tmax:达峰时间;Vz:统计矩计算的表观分布容积;CLz:统计矩计算的清除率;Cmax:峰浓度;Clast:尾点血药浓度。 3. 讨论
家兔经口染毒PQ的LD50为50 mg/kg [7]。前期预实验结果显示:对家兔以50 mg/kg或100 mg/kg剂量的PQ灌胃染毒时,家兔无明显中毒反应,200 mg/kg剂量的PQ染毒时家兔可见进食减少但尚未见死亡,400 mg/kg剂量的PQ染毒时家兔全部死亡。GB/T 21750—2008《化学品毒物代谢动力学实验》中要求各剂量组动物不少于4只,为保证在观察期内有足够的存活家兔数,本次实验中分配了8只家兔至高剂量染毒组,6只家兔至低剂量染毒组。
本研究结果显示两组家兔染毒后10 min血浆中即可检测到PQ,表明消化道吸收PQ非常迅速,染毒后1 ~ 2 h左右其血浆PQ浓度可达峰值,随后血浆PQ浓度迅速降低,24 h后血浆中的PQ均已降低到较低的水平。两组家兔血液中的PQ浓度随时间变化的趋势相似。TK参数显示随着染毒剂量由100 mg/kg增大到200 mg/kg,体内毒物的总负荷量增大,但不同染毒剂量下两组达峰时间和平均留存时间差异无统计学意义(P > 0.05)。另外,同组内各实验动物之间同时点血浆中PQ浓度和TK参数差别较大,特别是计算房室模型参数时变异更为明显,反映PQ水剂在家兔消化道的吸收速度和效率有明显的个体差异。
本研究结果显示的家兔血浆PQ变化趋势(浓度-时间曲线)与以往的文献报道基本相同[8-11]。然而,阚歆等[8]报道家兔经口染毒剂量为60 mg/kg时,血浆PQ峰浓度高达14 mg/L,病死率为16%;黄晓亮等[9]报道家兔经口染毒剂量为100 mg/kg时,血浆PQ峰浓度可达7.2 mg/L;陆元兰[10]报道的灌胃染毒剂量为100 mg/kg时,血浆PQ峰浓度为仅为1.7 mg/L,病死率则高达100%。曾薇[11]报道家兔经口染毒剂量为300 mg/kg时,血浆PQ峰浓度虽仅为3.5 mg/L,但病死率高达100%。上述结果与本研究在PQ峰浓度和中毒病死率方面有明显的差异,可能与TK实验采血点的设计、实验观察时间的长短、家兔间个体差异有关,也可能与各实验使用的PQ水剂品牌不同以及样品的前处理与检测PQ的方法不同有关。一般认为口服剂量估测和血药浓度检测在PQ中毒中具有重要作用,PQ中毒程度与摄入的剂量呈正相关,人体PQ摄入量> 40 mg/kg即可引起急性暴发性中毒,摄入量20 ~ 40 mg/kg即可引起中、重度中毒,摄入量 < 20 mg/kg表现为轻度中毒[12],但本研究结果提示单纯以口服剂量和血浆中PQ浓度预测预后仍具有一定的局限性。
传统TK动物实验多以大小鼠等啮齿类动物为实验动物,非啮齿类动物多选择比格犬等大动物进行。大小鼠体型较小,耐受采血量也较少,不适合毒性高、血药浓度低、检测采血量要求大的毒物TK实验。比格犬价格较贵,饲养条件较为苛刻,也限制了使用范围。以家兔为实验动物的TK实验发现,家兔体型较大,性情温顺,便于灌胃操作,耳中央动脉可以耐受多次较大量的采血,适用于毒性高、血药浓度低的毒物TK实验,也较易开展消化道毒物清除、血液净化实验等后续实验操作[13]。但是同时也观察到家兔个体遗传背景差异较明显,经口染毒时毒物吸收、代谢、排泄变异较大,影响测定TK参数的准确性和稳定性。
综上,本研究获得了不同染毒剂量下PQ在家兔体内的浓度-时间曲线和毒物代谢动力学参数,构建的TK模型与暴露后的TK参数相拟合,能较好地描述血浆中PQ浓度随时间的变化规律,研究结果为后续研究提供了基础性数据。
作者声明 本文无实际或潜在的利益冲突 -
表 1 PQ及内标物的多反应监测条件
化合物 母离子m/z 子离子m/z 去簇电压/v 碰撞能量/ eV PQ 171.2 155.2 85 40 77.2 85 52 PQ-d8 179.2 162.2 85 43 82.2 85 52 表 2 PQ的毒物代谢动力学房室模型参数
参数 单位 染毒剂量/(mg/kg) t值 P值 100 200 AUC(0 ~ t) mg/(L·h) 19.23 ± 14.21 63.54 ± 42.56 - 2.419 0.036 AUC(0 ~ ∞) mg/(L·h) 19.75 ± 14.23 65.00 ± 42.81 - 2.457 0.034 t1/2α h 1.09 ± 1.86 1 156.13 ± 2 829.33 - 1.000 0.363 t1/2β h 2 424.76 ± 3 500.85 4 631.29 ± 3 563.47 - 1.082 0.305 t1/2γ h 5.50 ± 4.14 -4 168.55 ± 10 222.88 1.000 0.363 V1 L/kg 1 488.04 ± 2 382.90 641.41 ± 1 167.72 0.779 0.454 V2 L/kg (-8.40 ± 20.59)× 108 (-1.09 ± 2.68)×107 - 0.987 0.369 V3 L/kg (8.55 ± 20.95)× 108 (2.05 ± 6.60)×106 0.998 0.364 CL1 L/(h·kg) 2 312.44 ± 3 900.34 1 359.86 ± 2 477.70 0.505 0.625 CL2 L/(h·kg) (-3.46 ± 8.46)× 106 -1 345.81 ± 3 212.53 - 1.000 0.363 CL3 L/(h·kg) (3.45 ± 8.46)×106 301.51 ± 628.66 1.000 0.363 K10 1/h 1.28 ± 0.41 59.81 ± 145.44 - 0.986 0.369 K12 1/h -621.15 ± 1 526.27 -76.03 ± 180.97 - 0.869 0.405 K21 1/h 1.77 ± 2.46 0.07 ± 0.08 1.695 0.151 K31 1/h 0.07 ± 0.09 0.01 ± 0.01 1.865 0.120 K13 1/h 622.96 ± 1 525.13 17.79 ± 35.33 0.972 0.376 Ka 1/h 2.44 ± 2.06 1.72 ± 1.47 0.704 0.498 t1/2ka 1/h 0.90 ± 1.37 0.75 ± 0.70 0.230 0.823 Tmax h 1.96 ± 2.41 1.76 ± 1.10 0.181 0.860 Cmax mg/L 2.37 ± 0.82 7.56 ± 3.14 - 3.918 0.009* 注:AUC:血药浓度-时间曲线下面积;t1/2α:中央室半衰期;t1/2β:第一周边室半衰期;t1/2γ:第二周边室半衰期(消除半衰期);V1:中央室表观分布容积;V2:第一周边室表观分布容积;V3:第二周边室表观分布容积;CL1:中央室清除率;CL2:第一周边室清除率;CL3:第二周边室清除率;K:速率常数;Ka:吸收速率常数;t1/2ka:吸收半衰期;Cmax:峰浓度;Tmax:达峰时间。 表 3 PQ的毒物代谢动力学非房室模型统计矩参数
参数 单位 染毒剂量/(mg/kg) t值 P值 100 200 AUC(0~t) mg/(L·h) 14.06 ± 3.19 72.89 ± 35.15 - 4.083 0.009 AUC(0~∞) mg/(L·h) 14.10 ± 3.21 76.05 ± 34.30 - 4.404 0.007 AUMC(0~t) h2·mg/L 171.50 ± 88.72 993.68 ± 325.32 - 5.972 0.009 AUMC(0~∞) h2·mg/L 175.02 ± 92.99 1356.91 ± 585.59 - 4.883 0.004 MRT(0~t) h 12.09 ± 5.14 14.43 ± 3.17 0.900 0.365 MRT(0~∞) h 12.28 ± 5.23 19.03 ± 8.42 - 1.659 0.128 VRT(0~t) h2 217.79 ± 210.42 340.65 ± 145.82 - 1.175 0.267 VRT(0~∞) h2 230.72 ± 222.02 813.79 ± 771.92 - 1.778 0.127 λz 1/h 0.08 ± 0.01 0.07 ± 0.04 0.717 0.500 t1/2z h 8.41 ± 1.89 15.47 ± 12.11 - 1.140 0.215 Tmax h 1.33 ± 0.41 2.16 ± 1.47 - 1.336 0.232 Vz L/kg 89.88 ± 26.04 67.36 ± 55.40 0.902 0.388 CLz L/(h·kg) 7.49 ± 2.19 2.98 ± 0.99 4.600 0.001 Cmax mg/L 2.53 ± 0.84 9.21 ± 4.43 - 3.629 0.013 Clast mg/L 0.002 ± 0.003 0.07 ± 0.09 - 1.910 0.114 注:AUC:血药浓度-时间曲线下面积;AUMC:血药浓度一阶矩时间曲线下面积;MRT:平均滞留时间;VRT:平均滞留时间方差;λz:尾点斜率;t1/2z:统计矩计算的半衰期;Tmax:达峰时间;Vz:统计矩计算的表观分布容积;CLz:统计矩计算的清除率;Cmax:峰浓度;Clast:尾点血药浓度。 -
[1] DINIS-OLIVEIRA R J, DUARTE J A, SANCHEZ-NAVARRO A, et al. Paraquat poisonings: mechanisms of lung toxicity, clinical features, and treatment[J]. Crit Rev Toxicol, 2008, 38(1): 13-71. doi: 10.1080/10408440701669959
[2] YIN Y, GUO X, ZHANG S L, et al. Analysis of paraquat intoxication epidemic (2002-2011) within China[J]. Biomed Environ Sci, 2013, 26(6): 509-512. http://europepmc.org/abstract/MED/23816587
[3] 中华人民共和国农业部, 工业和信息化部, 国家质量监督检验检疫总局. 农业部、工业和信息化部、国家质量监督检验检疫总局公告第1745号[EB/OL]. (2012-04-12)[2020-10-28]. http://www.zzys.moa.gov.cn/gzdt/201204/t20120427_6309814.htm. [4] 刘琴. 百草枯水剂屡现市场令人忧敌草快"变脸"冒充弊端多[J]. 农药市场信息, 2017(22): 17-19. http://www.cnki.com.cn/Article/CJFDTotal-NYSC201722022.htm [5] 孙宝迪, 袁雪丰, 聂时南. 临床需警惕与敌草快中毒伴随的百草枯中毒(附二例报告)[J]. 临床误诊误治, 2018, 31(4): 64-66. https://www.cnki.com.cn/Article/CJFDTOTAL-LCWZ201804022.htm [6] 中国国家标准化管理委员会, 中华人民共和国国家质量监督检验检疫总局. 实验动物环境及设施: GB 14925-2010[S]. 北京: 中国标准出版社, 2010. [7] WHO. Pesticide Residues in Food: Paraquat[EB/OL]. (2015-02-23)[2020-10-28]. http://www.inchem.org/pages/jmpr.html.
[8] 阚歆, 张潇云, 董洁, 等. 百草枯在兔体内的毒物代谢动力学[J]. 中华劳动卫生职业病杂志, 2010, 28(10): 756-759. doi: 10.3760/cma.j.issn.1001-9391.2010.10.014 [9] 黄晓亮, 李映新, 凌家杰, 等. 高效液相色谱法测定兔灌胃后血清中百草枯浓度及其变化特征[J]. 中国现代医学杂志, 2018, 28(13): 17-21. https://www.cnki.com.cn/Article/CJFDTOTAL-ZXDY201813004.htm [10] 陆元兰. 漂白土洗胃联合清胰Ⅱ号导泻对兔口服百草枯中毒的治疗观察[D]. 遵义: 遵义医学院, 2014. [11] 曾薇. 洗胃对兔口服百草枯急性中毒治疗作用的探讨[D]. 成都: 四川大学, 2004. [12] 中国医师协会急诊医师分会. 急性百草枯中毒诊治专家共识(2013)[J]. 中国急救医学, 2013, 33(6): 484-489. https://www.cnki.com.cn/Article/CJFDTOTAL-LCWZ201412002.htm [13] 郭翔, 刘奋, 钟才高, 等. 家兔毒死蜱染毒的毒物代谢动力学研究[J]. 毒理学杂志, 2019, 33(4): 314-318. https://www.cnki.com.cn/Article/CJFDTOTAL-WSDL201904011.htm





 下载:
下载: