Diagnostic significance of combined detection of serum indexes in severe heatstroke: a clinical analysis of 70 patients with severe heatstroke
-
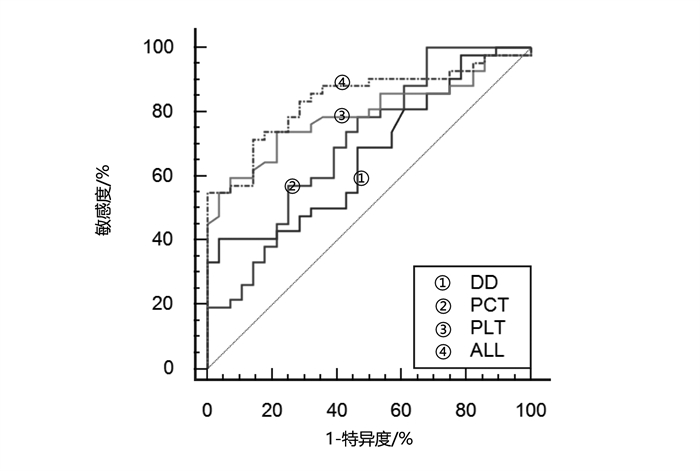
+ English摘要:目的 通过分析重症中暑患者的临床特征,探讨热射病(heat stroke,HS)辅助诊断的早期敏感临床指标,以期及早干预病情。方法 选择南通大学第二附属医院收治的70例重症中暑住院患者为研究对象,根据患者中暑的严重程度,分为热痉挛与热衰竭组(n = 28)、劳力型热射病(exertional heat stroke,EHS)组(n = 24)、经典型热射病(classic heat stroke,CHS)组(n = 18)。记录患者的一般资料及入院24 h的临床检验指标,比较各组患者临床指标的差异,进一步绘制热痉挛与热衰竭组和HS组的受试者工作特征曲线(ROC)。结果 70例患者中男性46例,女性24例;平均年龄(65.72 ± 16.64)岁。最高体温(39.66 ± 1.08)℃,住院时间(15.58 ± 14.49)d。61例病情好转,9例死亡。3组患者入院24 h内多项临床指标差异有统计学意义(P < 0.05)。其中:EHS组及CHS组的体温高于热痉挛与热衰竭组(P < 0.05),但EHS组、CHS组的体温差异无统计学意义(P > 0.05);EHS组的D-二聚体(DD)、降钙素原(PCT)高于热痉挛与热衰竭组、CHS组(P < 0.05);EHS组的血小板(PLT)、超敏C反应蛋白(CRP)、血钠(Na)、静脉血糖(GLU)、APACHEⅡ低于热痉挛与热衰竭组、CHS组(P < 0.05),PLT的降低最为显著;CHS组糖化血红蛋白(HbA1C)高于热痉挛与热衰竭组、EHS组(均P < 0.05)。各指标在热痉挛与热衰竭组、HS组患者间的受试者工作特征曲线显示:各指标均无法同时达到较高的特异度和敏感度;而串联DD、PCT、PLT三者后的AUC上升至0.838(95% CI:0.731 ~ 0.916),敏感度为71.43%,特异度为85.71%,该联合指标的诊断效能高于任何单一指标。结论 PLT的显著下降、PCT和DD的增高可能是HS的早期敏感指标,三者联合检测可作为HS早期诊断以及病情危重的参考依据。
-
一氧化碳(carbon monoxide,CO)是一种无色、无味、无刺激性的窒息性气体,主要由含碳有机物不完全燃烧产生,是日常生产生活中常见的有毒有害性气体之一[1],生产生活中以急性一氧化碳中毒多见[2-3]。CO入血之后80% ~ 90%与血红蛋白结合,形成碳氧血红蛋白,降低了血液携氧和输氧的能力[4],长期的缺氧将严重损伤中枢神经系统(central nervous system,CNS)的功能[5]。一部分急性一氧化碳中毒的患者在意识障碍恢复后,经过2 ~ 60 d的“假愈期”,可出现急性一氧化碳中毒迟发性脑病(delayed encephalopathy after acute carbon monoxide poisoning,DEACMP)[6-7]。研究表明,急性DEACMP的发生率高达45% [8-9]。目前临床上针对DEACMP尚缺乏有效的治疗手段,主要是高压氧疗辅助药物治疗。目前认为可能导致该病发生的几种机制包括:缺血缺氧损伤和细胞凋亡机制;免疫损伤神经脱髓鞘机制;再灌注损伤和自由基机制;神经递质异常学说;基因易感性和其他[10]。
谷氨酸(glutamate,Glu)是哺乳动物中枢神经系统主要的兴奋性神经递质,对维持大脑皮层的兴奋性具有重要意义。Glu由突触前膜释放,作用于突触后膜上相应的谷氨酸受体而发挥作用。谷氨酸受体分为离子型受体和代谢型受体两种,其中离子型谷氨酸受体又分为N-甲基-D-天冬氨酸(NMDA)受体和非NMDA受体。研究表明,谷氨酸信号通路在学习、记忆、神经生长发育和突触的可塑性方面发挥着重要作用[11]。病理条件下,产生过量的谷氨酸使谷氨酸受体过度激活,对神经系统产生兴奋毒性,引发神经组织细胞的功能障碍甚至死亡[12]。
PC12细胞是源于大鼠肾上腺髓质嗜铬细胞瘤的一种细胞系,被广泛用于神经系统的相关疾病的体外研究。外源性的一氧化碳释放分子2(CORM-2)是一种新型的CO供体,溶解于二甲基亚砜(DMSO)溶剂中时,可稳定和缓慢地释放出CO气体。本实验将以PC12细胞为研究对象,以CORM-2为CO供体,建立CO神经损伤的体外模型,探究外源性CO对PC12细胞谷氨酸系统的影响和可能机制,为一氧化碳中毒迟发性脑病的治疗提供实验依据。
1. 材料与方法
1.1 材料
1.1.1 主要试剂
胎牛血清(以色列Biological Industries公司);CORM-2(美国GLPBIO公司);MTS细胞活性测定试剂盒(上海信裕生物工程有限公司);兔抗NR1多克隆抗体(美国Abcam公司);兔抗NR2A多克隆抗体(美国Abcam公司);兔抗NR2B多克隆抗体(美国Abcam公司);兔抗β-actin多克隆抗体(美国Abcam公司);ECL发光试剂盒(美国Millipore公司);预染蛋白Marker(上海雅酶生物科技有限公司);Fluo-2,AM(北京索莱宝有限公司);二喹啉甲酸(bicinchoninic acid,BCA)蛋白浓度测定试剂盒(北京鼎国昌盛生物技术公司);谷氨酸比色法测试盒(武汉Elabscience公司)等。
1.1.2 主要仪器
二氧化碳培养箱(上海Heal Force公司),蛋白质电泳装置(美国Bio-Rad公司),干式恒温器(杭州奥盛仪器有限公司),全自动酶标仪(美国Labsystems公司),-40 ℃低温冰箱(美国Thermo公司)等。
1.2 方法
1.2.1 细胞分组与处理
PC12细胞于37 ℃,体积分数5%的CO2条件下培养至状态稳定后,经细胞消化,用DMEM培养基调节细胞浓度为4 × 105/mL接种至96孔板中,待细胞铺满80% ~ 90%时,分别以0 ~ 400 μmol/L的CORM-2对其进行染毒。根据MTS法检测细胞活力结果确定合适的染毒浓度,最终实验设置对照组、200 μmol/L CORM-2组、250 μmol/L CORM-2组、300 μmol/L CORM-2组,培养12 h,染毒结束后用蛋白免疫印迹试验分别检测NR1、NR2B蛋白的表达水平,用比色法检测谷氨酸的含量,荧光探针法检测钙离子浓度。
1.2.2 用Western Blotting法检测目的蛋白相对表达水平
CORM-2染毒PC12细胞后,去除培养基,用磷酸缓冲盐溶液(phosphate buffered saline,PBS)洗3遍,加入细胞裂解液,冰上裂解40 min,并用细胞刮将裂解好的细胞刮落,收集细胞至EP管中,4 ℃下12 000 r/min离心20 min,取上清,置- 20 ℃保存。BCA法测定上清液中蛋白浓度,并调整各标本至相同蛋白浓度。蛋白样品经聚丙烯酰胺凝胶电泳,转膜,磷酸盐吐温缓冲液(PBST)浸泡,封闭,PBST洗膜,分别加入相应的一抗NR1(1∶1 000稀释),NR2B(1∶1 000稀释),4 ℃孵育过夜,PBST洗膜,加入相应二抗山羊抗兔(1∶5 000稀释),孵育2 h,PBST洗膜3次,ECL试剂盒显色。
1.2.3 细胞内Ca2+含量测定
按上述方法培养PC12细胞,经不同浓度CORM-2暴露12 h后去除培养基,用预冷的D-hanks溶液洗涤细胞3次后收集细胞,加入1 mL D-hanks溶液,预温37 ℃,加入5 μL的Fura-2/AM工作液,置于37 ℃恒温振荡培养箱中,避光孵育30 ~ 45 min。用D-hanks溶液洗涤细胞3次,置于37 ℃恒温振荡培养箱中避光孵育30 min。荧光酶标仪检测细胞,激发波长380 nm和340 nm,发射波长510 nm。细胞内游离Ca2+浓度采用公式(1)计算:
$$ {\left( {{\rm{C}}{{\rm{a}}^{2 + }}} \right)_{\rm{I}}} = {K_{\rm{d}}} \times \left( {F - {F_{\min }}} \right)/\left( {{F_{\max }} - F} \right) $$ (1) 式中:Kd值为224 nmol/L;Fmax为最大的荧光比值,以10% Triton - X100测得;Fmin为最小的荧光比值,在Fmax基础上加入EGTA后所测得;F为340 nm、380 nm的荧光比值。
1.2.4 统计学分析
所有实验数据均使用统计分析软件SPSS 20.0进行数据处理分析,正态分布资料用均数±标准差(x ± s)表示。组间比较采用单因素方差分析,进一步的两两组间比较采用SNK法,以P < 0.05为差异有统计学意义。
2. 结果
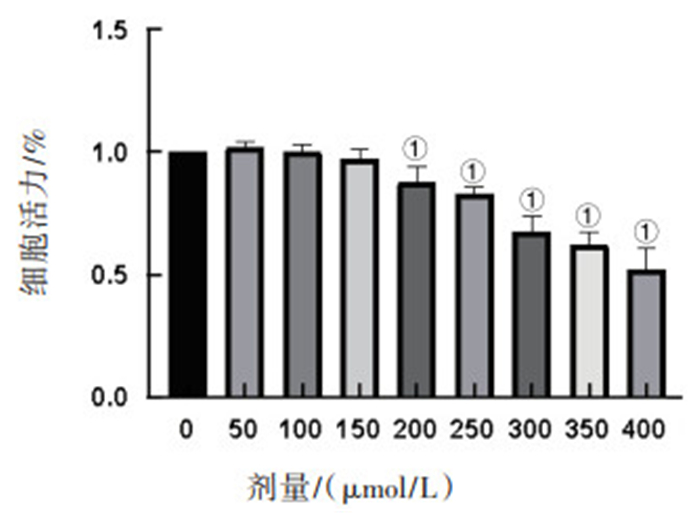
2.1 MTS法检测细胞活力
当CORM-2浓度<200 μmol/L时,PC12细胞存活率与对照组相比差异无统计学意义(P>0.05);CORM-2浓度≥ 200 μmol/L时,PC12细胞存活率明显下降,与对照组相比,差异均有统计学意义(P<0.05)。见图 1。
2.2 CORM-2对内谷氨酸受体NR1和NR2B蛋白表达的影响
染毒12 h后,各剂量与对照组相比,NMDA受体的NR1亚基的表达未发生显著变化,说明CORM-2处理对NR1亚基的表达没有显著影响;染毒12 h后,随着染毒剂量的增加,NR2B亚基的表达也随之增加,当CORM-2浓度为250 μmol/L和300 μmol/L时,与对照组相比,细胞内的NR2B亚基含量显著升高,差异具有统计学意义(P < 0.05),且250 μmol/L和300 μmol/L两组间相比,NR2B亚基的表达水平差异也有统计学意义(P < 0.05)。见图 2、表 1。
表 1 各组PC12中NR1和NR2B蛋白相对表达水平比较(x ± s) 组别 重复次数 NR1 NR2B 对照组 4 1.41 ± 0.18 0.99 ± 0.21 200 μmol/L 4 1.37 ± 0.23 1.14 ± 0.18 250 μmol/L 4 1.29 ± 0.20 1.24 ± 0.13① 300 μmol/L 4 1.28 ± 0.13 1.61 ± 0.18①②③ F值 0.46 13.63 P值 > 0.05 < 0.01 注:①与对照组比较,P < 0.05;②与200 μmol/L剂量组比较,P < 0.05;③与250 μmol/L剂量组比较,P < 0.05。 2.3 谷氨酸浓度检测
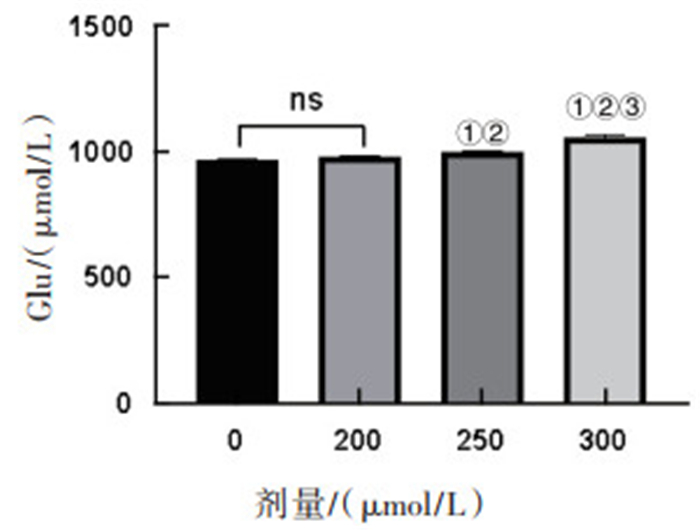
CORM-2处理12 h后,对照组、200 μmol/L、250 μmol/L和300 μmol/L染毒组Glu含量分别为(968.75 ± 11.09)μmol/L、(977.50 ± 4.08)μmol/L、(995.00 ± 9.57)μmol/L和(1047.50 ± 15.81)μmol/L。与对照组和200 μmol/L染毒组相比,250 μmol/L和300 μmol/L染毒组细胞释放的谷氨酸的浓度水平显著上升,并随染毒剂量的增加而增加,差异具有统计学意义(P < 0.05)。见图 3。
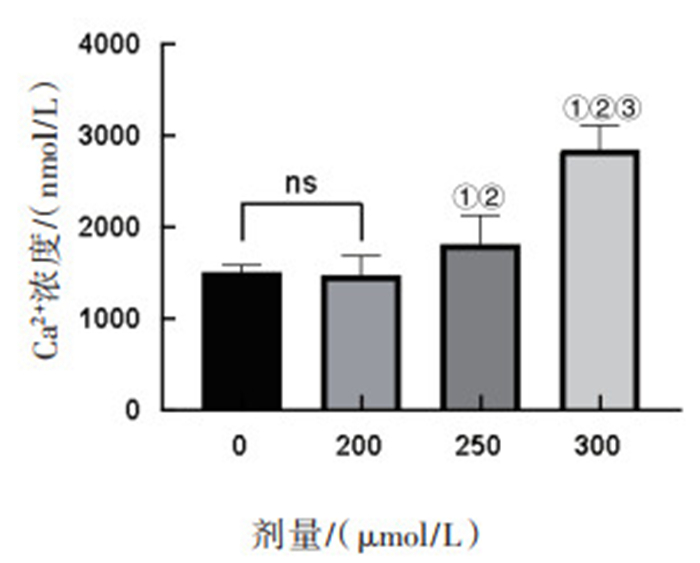
2.4 细胞内Ca2+浓度测定
如图 4所示,CORM-2处理12 h后,对照组、200 μmol/L、250 μmol/L和300 μmol/L染毒组Ca2+浓度分别为(1 497.89 ± 91.67)nmol/L、(1 465.23 ± 228.11)nmol/L、(1 945.90 ± 164.84)nmol/L和(2 844.47 ± 262.96)nmol/L。与对照组和200 μmol/L染毒组相比,250 μmol/L和300 μmol/L染毒组细胞内Ca2+浓度水平显著上升,并随染毒剂量的增加而增加,差异有统计学意义(P < 0.05)。
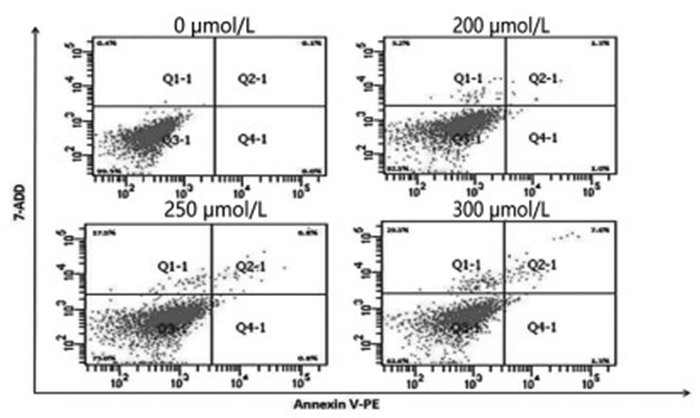
2.5 流式细胞术检测细胞凋亡
如图 5所示,CORM-2处理12 h后,对照组、200 μmol/L、250 μmol/L和300 μmol/L染毒组细胞凋亡比例分别为(0.13 ± 0.06)、(2.83 ± 1.46)、(7.17 ± 1.10)和(7.37 ± 0.25)。与对照组相比,200 μmol/L、250 μmol/L和300 μmol/L染毒组细胞凋亡水平显著上升,并随染毒剂量的增加而增加,差异具有统计学意义(P < 0.05)。
3. 讨论
目前,一氧化碳对神经系统损伤的发病机制尚未完全阐明,尤其是其特有的迟发性脑病的病因尚不明确。CO是新发现的除一氧化氮(NO)以外,体内又一种重要的气态信号分子。生理条件下,体内也会产生一定量的内源性CO,主要由血红素氧合酶(HO)代谢血红素产生[13]。其分子结构与NO相似,可通过与NO相似的作用机制发挥与之类似的生理调节作用,但在缺血缺氧等应激因素的刺激下,诱导型血红素氧合酶(HO-1)大量表达,致使内源性CO的量超过生理水平而发挥损害作用。
NMDA受体广泛分布于中枢神经系统中,因涉及学习、记忆和神经退行性疾病等各种生理病理过程而备受关注。NMDA受体主要由NR1和NR2两个亚单位构成,NR1是基本功能单位,含有甘氨酸和Ca2+通道的结合位点;而NR2是其调节单位,含有谷氨酸结合位点[14],因此,PC12细胞中NR1和NR2亚单位的表达水平可影响NMDA受体的功能,进而影响PC12细胞膜对Ca2+的通透性[15]。PC12细胞内Ca2+浓度的变化对谷氨酸信号通路的激活具有重要的调控作用,与谷氨酸的兴奋毒性密切相关。研究还发现,NR1/NR2A和NR1/NR2B是NMDA受体的主要组合形式,而含有NR2B亚基的NMDA受体与神经元兴奋毒性的关系更为密切[16],因此本实验决定检测谷氨酸、NR1/NR2B亚基来探究CORM-2处理对PC12细胞谷氨酸信号通路的影响。本研究结果显示,与对照组比较,浓度为250和300 μmol/L的CORM-2刺激,均可引起PC12细胞释放谷氨酸的含量和NR2B的蛋白的表达上调(P < 0.05);且250和300 μmol/L两个剂量组间,谷氨酸含量和NR2B表达情况的差异也具有统计学意义(P < 0.05),提示CORM-2处理激活了PC12细胞的谷氨酸信号通路。
Ca2+是细胞内一种重要的第二信使,细胞内的钙稳态对维持细胞的正常活性和生理功能具有重要意义。大量动物研究表明,CO中毒可引起谷氨酸的过度释放,过量的谷氨酸使突触后膜上的NMDA受体过度激活,进而引发Ca2+大量内流而使细胞钙超载。CO中毒时,缺氧导致神经组织无氧代谢增加,使得乳酸产生增多,而细胞内H+浓度增加也会破坏钙稳态[17]。研究发现,神经组织在缺血缺氧时,细胞钙超载与神经细胞死亡联系密切[18];神经退行性疾病与神经组织细胞内长期内质网应激(ERS)启动凋亡通路而引发的细胞死亡密切相关。目前多认为外界干扰所引起的细胞钙超载是引发细胞凋亡的始动因素,细胞内Ca2+水平异常升高会引发一系列的级联反应,最终导致细胞坏死或凋亡[19]。本研究发现,与对照组和低剂量组相比,中、高剂量(250 μmol/L、300 μmol/L)染毒12 h后,细胞内Ca2+浓度随着染毒剂量的增加而增加,细胞凋亡率逐渐增加,细胞内Ca2+水平的变化与谷氨酸及其受体含量的变化同向,且Ca2+水平变化与细胞活性的变化反向。
综上所述,本研究结果显示外源性CORM-2暴露可引起PC12细胞谷氨酸释放增加,NMDA受体表达上调,从而引起细胞内Ca2+浓度增加,干扰了细胞内钙稳态环境,进而导致细胞凋亡。以上结果为揭示一氧化碳中毒迟发性脑病的机制提供了实验参考依据。
作者声明 本文无实际或潜在的利益冲突 -
表 1 3组患者入院24 h内临床资料比较
变量 热痉挛与热衰竭(n= 28) EHS(n = 24) CHS(n = 18) χ2、F或Z值 P值 年龄/岁 66.89 ± 14.83 64.08 ± 21.46 66.11 ± 12.68 0.183 0.833 性别例数(男/女) 20/8 16/8 10/8 1.240 0.538 起病时间/h 22(40) 24(36) 23(42) 0.796 0.672 住院天数/d 13.57 ± 9.41 15.46 ± 17.82 18.83 ± 16.62 0.707 0.497 Tmax / ℃ 38.73 ± 0.49 40.71 ± 0.58 ① 40.64 ± 0.69 ① 97.020 < 0.001 DD/(μg/mL) 1 880.00(3 365.25) 10 946.00(11 265.00)① 2 110.00(3 497.50)② 10.160 0.006 WBC/(×109/L) 11.66 ± 5.38 9.16 ± 3.46 10.80 ± 4.12 2.026 0.140 N/(×109/L) 8.94 ± 3.23 7.34 ± 2.33 9.53 ± 3.81② 2.897 0.620 Hb /(g/L) 127.21 ± 24.77 123.83 ± 18.20 122.94 ± 14.16 0.299 0.743 PCT/(ng/L) 1.79(9.81) 21.98(57.97)① 2.88(8.28)② 15.204 < 0.001 PLT/(×109/L) 113(74.75) 40(16)① 100.5(91.50)② 35.515 < 0.001 ESR/(mm) 13(24.75) 23(20) 18(22.75) 2.834 0.242 CRP/(mg/L) 39.98(130.60) 13(13.56)① 38.84(78.96)② 7.927 0.019 pH值 7.41 ± 0.06 7.39 ± 0.09 7.40 ± 0.86 0.190 0.827 LAC/(mmol/L) 3.41 ± 1.45 2.88 ± 1.45 2.88 ± 0.99 1.319 0.274 SPO2/% 93.74 ± 4.36 95.57 ± 3.98 93.78 ± 5.81 0.946 0.393 K /(mmol/L) 4.1(0.93) 3.56(1.40) 3.7(0.74) 1.685 0.431 Na/(mmol/L) 139.31 ± 8.13 128.77 ± 28.33① 140.97 ± 5.86 ② 3.227 0.046 Cl/(mmol/L) 104.99 ± 8.52 97.86 ± 22.35 103.78 ± 6.65 1.674 0.195 AB/(mmol/L) 20.31 ± 4.08 22.78 ± 4.50 22.02 ± 3.91 2.376 0.101 GLU/(mmol/L) 7.166(3.82) 5.95(1.95)① 7.45(5.68)② 6.300 0.043 HbA1C/% 5.85 ± 0.74 5.62 ± 0.67 7.09 ± 2.04 ①② 8.701 < 0.001 TNI/(ng/mL) 0.120(0.90) 0.145(1.30) 0.125(0.60) 2.015 0.365 Myo/(ng/mL) 341(653.75) 677(860.88) 469(715.93) 1.897 0.387 CKMB/(ng/mL) 25.5(38.25) 48(40) 29.5(38.65) 2.435 0.296 BNP/(ng/L) 1 055.2(1 252.55) 975.1(3187) 453.5(1 275.58) 1.192 0.551 ALT/(U/L) 41.5(41) 34(49) 52.5(94.25) 4.159 0.125 AST/(U/L) 50.5(52) 69(101) 76(63.5) 2.449 0.294 SCR/(mmol/L) 86.0(73.3) 81.0(93.0) 80.5(51.8) 0.783 0.676 BUN/(mmol/L) 8.11(5.22) 6.53(4.73) 7.85(8.73) 0.512 0.774 APACHEⅡ分值 16.25 ± 6.94 14.13 ± 5.55 21.83 ± 9.54 ①② 5.973 0.004 注:①与热痉挛与热衰竭组比较,P<0.05;②与EHS组比较,P<0.05。符合正态分布的年龄、住院时间、体温、WBC、N、Hb、PH、LAC、SPO2、Na、Cl、AB、HbA1C,以均数±标准差(x ± s)表示;符合偏态分布的如起病时间、DD、PCT、PLT、ESR、CRP、K、GLU、TNI、Myo、CKMB、BNP、ALT、AST、SCR、BUN,以M(P75 - P25值)表示。 表 2 临床相关指标对重症中暑早期诊疗预测价值
变量 灵敏度/% 特异度/% 约登指数 AUC值 95%CI值 CRP/(mg/L) 95.24 32.14 0.273 8 0.588 0.464 ~ 0.704 Na/(mmol/L) 26.19 89.29 0.154 8 0.578 0.454 ~ 0.695 GLU/(mmol/L) 40.48 85.71 0.261 9 0.597 0.472 ~ 0.712 HbA1C/% 35.71 82.14 0.178 6 0.541 0.418 ~ 0.661 APACHEⅡ分值 85.71 0 0.142 9 0.512 0.390 ~ 0.634 DD/(μg/mL) 40.48 96.43 0.369 0 0.670 0.547 ~ 0.777 PCT/(ng/L) 100 32.14 0.321 4 0.705 0.584 ~ 0.808 PLT/(×109/L) 73.81 78.57 0.523 8 0.791 0.677 ~ 0.879 DD+PCT+PLT 71.43 85.71 0.571 4 0.838 0.731 ~ 0.916 -
[1] ZHANG W, HUO F J, YUE Y K, et al. Heat stroke in cell tissues related to sulfur dioxide level is precisely monitored by light-controlled fluorescent probes[J]. J Am Chem Soc, 2020, 142(6): 3262-3268. doi: 10.1021/jacs.9b13936
[2] TOLLEFSON J. Global-warming limit of 2℃ hangs in the balance[J]. Nature, 2015, 520(7545): 14-15. doi: 10.1038/nature.2015.17202
[3] EPSTEIN Y, YANOVICH R. Heat stroke[J]. N Engl J Med, 2019, 380(25): 2449-2459. doi: 10.1056/NEJMra1810762
[4] 中华人民共和国卫生部. 职业性中暑诊断标准: GBZ 41-2002[S]. 北京: 中国标准出版社, 2002. [5] 刘树元, 宋景春, 毛汉丁, 等. 中国热射病诊断与治疗专家共识[J]. 解放军医学杂志, 2019, 44(3): 181-196. https://www.cnki.com.cn/Article/CJFDTOTAL-JFJY201903001.htm [6] NELLAIAPPAN S, MANDALI P K, PRABAKARAN A, et al. Electrochemical immunosensors for quantification of procalcitonin: progress and prospects[J]. Chemosensors, 2021, 9(7): 182. doi: 10.3390/chemosensors9070182
[7] 范华杰, 牛磊. 中暑患者血清心肌酶水平变化与患者病情判断及预后的关系[J]. 解放军预防医学杂志, 2018, 36(3): 298-300. https://www.cnki.com.cn/Article/CJFDTOTAL-JYYX201803002.htm [8] VERGARO G, GENTILE F, MEEMS L M G, et al. NT-proBNP for risk prediction in heart failure: identification of optimal cutoffs across body mass index categories[J]. JACC Heart Fail, 2021, 9(9): 653-663. doi: 10.1016/j.jchf.2021.05.014
[9] 王鸿利, 王学锋. D-二聚体检测的方法及其临床应用[J]. 中华医学杂志, 2004, 84(2): 171-173. doi: 10.3760/j:issn:0376-2491.2004.02.024 [10] 闫福, 施长苗, 罗康, 等. 浙江长兴2016-2018年高温中暑病例流行病学特征分析[J]. 中国公共卫生管理, 2020, 36(3): 419-423. https://www.cnki.com.cn/Article/CJFDTOTAL-GGWS202003039.htm [11] 潘梅竹, 许慧慧, 东春阳, 等. 2013-2017年上海重症中暑病例死亡的相关因素分析[J]. 中华预防医学杂志, 2019, 53(1): 93-96. doi: 10.3760/cma.j.issn.0253-9624.2019.01.013 [12] PEIRIS A N, JAROUDI S, NOOR R. Heat stroke[J]. JAMA, 2017, 318(24): 2503. doi: 10.1001/jama.2017.18780
[13] HIFUMI T, KONDO Y, SHIMIZU K, et al. Heat strok[J]. J Intensive Care, 2018(6): 30.
[14] FILEP E M, MURATAT Y, ENDRES B D, et al. Exertional heat stroke, modality cooling rate, and survival outcomes: a systematic review[J]. Medicina(Kaunas), 2020, 56(11): 589.
[15] WOODS S E. Immunosuppression is associated with epigenetic remodelling in a murine model of exertional heat stroke[J]. J Physiol, 2020, 599(1): 119-141.
[16] LEON L R, HELWIG B G. Heat stroke: role of the systemic inflammatory response[J]. J Appl Physiol, 2010, 109(6): 1980-1988. doi: 10.1152/japplphysiol.00301.2010
[17] WAGNER M, KAUFMANN P, FICKERT P, et al. Successful conservative management of acute hepatic failure following exertional heatstroke[J]. Eur J Gastroenterol Hepatol, 2003, 15(10): 1135-1139. doi: 10.1097/00042737-200310000-00013
[18] ALZEER A H, EL-HAZMI M A, WARSY A S, et al. Serum enzymes in heat stroke: prognostic implication[J]. Clin Chem, 1997, 43(7): 1182-1187. doi: 10.1093/clinchem/43.7.1182
[19] 陈峰. 血清PCT、CRP结合APACHEⅡ评分对感染性休克患者生存状况的评估效果[J]. 检验医学与临床, 2021, 18(1): 109-112. https://www.cnki.com.cn/Article/CJFDTOTAL-JYYL202101034.htm [20] 陈挺阳, 王喜泰. NT-proBNP及APACHE评分在老年慢性心力衰竭预后评估中的应用[J]. 临床合理用药杂志, 2020, 13(35): 175-177. https://www.cnki.com.cn/Article/CJFDTOTAL-PLHY202035084.htm [21] SCHEER C S, FUCHS C, GRUNDLING M, et al. Impact of antibiotic administration on blood culture positivity at the beginning of sepsis: a prospective clinical cohort study[J]. Clin Microbiol Infect, 2019, 25(3): 326-331. doi: 10.1016/j.cmi.2018.05.016
[22] 杨巧云, 左祥荣, 曹权. 降钙素原鉴别ICU重度颅脑损伤患者发热原因的价值探讨[J]. 实用临床医药杂志, 2012, 16(19): 120-121;126. https://www.cnki.com.cn/Article/CJFDTOTAL-XYZL201219044.htm [23] 余保军, 王黎, 彭娜, 等. HMGB1与重症中暑大鼠凝血紊乱的相关性分析[J]. 解放军医学杂志, 2020, 45(3): 292-297. https://www.cnki.com.cn/Article/CJFDTOTAL-JFJY202003011.htm [24] YIN H M, LU Y, SHI X Z, et al. Study on dynamic changes of platelet count and function in severe heatstroke rats[J]. Med J Chin PLA, 2018, 43(5): 398-402.
[25] ZHONG L, WU M, LIU Z, et al. Risk factors for the 90-day prognosis of severe heat stroke: a case-control study[J]. Shock, 2020, 55(1): 61-66.
[26] 李亚杰, 俞建峰, 周仪, 等. 早期血小板变化对重症中暑患者28d死亡的预测价值[J]. 天津医药, 2020, 48(4): 279-283. https://www.cnki.com.cn/Article/CJFDTOTAL-TJYZ202004009.htm [27] 李冰, 贾晔然, 高伟, 等. 重症中暑脑损伤患者神经元特异性烯醇化酶及脑活性肽100B蛋白的表达及意义[J]. 解放军医学杂志, 2020, 45(12): 1282-1287. doi: 10.11855/j.issn.0577-7402.2020.12.12 [28] YILMAZ M B, CIHAN G, GERAY Y, et al. Role of mean platelet volume in triaging acute coronary syndromes[J]. J Thromb Thrombolysis, 2008, 26(1): 49-54. doi: 10.1007/s11239-007-0078-9
[29] JINDAL S, GUPTA S, GUPTA R, et al. Platelet indices in diabetes mellitus: indicators of diabetic microvascular complications[J]. Hematology, 2011, 16(2): 86-89. doi: 10.1179/102453311X12902908412110
[30] GUCLU E, DURMAZ Y, KARABAY O. Effect of severe sepsis on platelet count and their indices[J]. Afr Health Sci, 2013, 13(2): 333-338.
[31] 唐劲松, 宣春, 林景涛, 等. C-反应蛋白、白介素-6及降钙素原检测在新冠肺炎中的临床意义[J]. 实用医学杂志, 2020, 36(7): 839-841. https://www.cnki.com.cn/Article/CJFDTOTAL-SYYZ202007002.htm [32] 郑焱, 郑芬萍, 李红. 住院患者低钠血症的患病率和病因分析[J]. 中华内科杂志, 2020, 59(1): 29-34. https://cdmd.cnki.com.cn/Article/CDMD-10335-1015615050.htm [33] 张霖, 周婉, 陈剑. 脓毒症糖代谢紊乱的发生机制及治疗[J]. 中华糖尿病杂志, 2020, 12(9): 753-755. [34] AMERICAN DIABETES ASSOCIATION. 2 classification and diagnosis of diabetes: standards of medical care in diabetes-2020[J]. Diabetes Care, 2020, 43(Suppl 1): S14-S31.
[35] 王彦光, 朱鸿斌, 徐维超. ROC曲线及其分析方法综述[J]. 广东工业大学学报, 2021, 38(1): 46-53. https://www.cnki.com.cn/Article/CJFDTOTAL-GDGX202101007.htm -
期刊类型引用(12)
1. 汤玉华,季晓庆,董秋. 南京市尘肺病患者直接经济负担及其影响因素分析. 职业卫生与应急救援. 2025(01): 27-30+86 .  本站查看
本站查看
2. 王艳艳,张莹,梁伟辉,曾子芳,李喜英. 金水宝联合汉防己甲素治疗尘肺病的疗效分析. 职业卫生与应急救援. 2024(02): 197-200 .  本站查看
本站查看
3. 米兆娟,陈超,刘薇,陈成龙,白林,阎西革. 烟台市尘肺病患者医疗费用及影响因素分析. 职业与健康. 2024(07): 865-868+873 .  百度学术
百度学术
4. 韩宜成,杨成新,何平,李雪丹,杨丹,李涛. 基于质性研究的新疆尘肺病康复站运行现状调查. 工业卫生与职业病. 2024(03): 253-257 .  百度学术
百度学术
5. 汪婷,王小皙,邱翠娟,张华东. 2013—2022年重庆市尘肺病患者发病变化趋势和疾病负担影响因素分析. 职业与健康. 2024(09): 1178-1183 .  百度学术
百度学术
6. 周雯,王玉,王平. 我国尘肺病护理与防治研究进展. 职业与健康. 2024(09): 1277-1281 .  百度学术
百度学术
7. 陈忠文,杨小红,杨婷婷,罗东,程淑群. 尘肺病康复项目纳入医疗保障服务现状分析. 现代医药卫生. 2024(12): 2151-2154 .  百度学术
百度学术
8. 韩宜成,杨倩,左书瑞,李雪丹,杨成新,何平. 尘肺病康复站患者康复治疗效果评价. 中国职业医学. 2024(02): 214-218 .  百度学术
百度学术
9. 陈焱,王永义,叶绿素. 尘肺病康复站41名工作人员呼吸康复培训的效果观察. 现代医药卫生. 2024(14): 2367-2370+2375 .  百度学术
百度学术
10. 叶梦娟,高峰,邱光文,甘俊英,周燕,彭必勤. 马鞍山市尘肺病患者生命质量及影响因素研究. 职业卫生与应急救援. 2024(04): 464-469 .  本站查看
本站查看
11. 范槐芳,王超群,苏晓珏,贾仰民,林华芳,卢亚飞. 隔药饼灸治疗肺气虚损型尘肺患者的疗效观察. 中国中医药科技. 2024(06): 1041-1042 .  百度学术
百度学术
12. 陈添良,罗添馨,张娅妮,黄永顺,杨铮. 尘肺病患者报告结局测定量表之特异模块条目的筛选. 山东医药. 2023(33): 45-49 .  百度学术
百度学术
其他类型引用(1)





 下载:
下载: